题目内容
18.主链上有4个碳原子的某烷烃有两种同分异构体,含有相同碳原子数且主链上也有4个碳原子的烯烃(含一个碳碳双键)的同分异构体有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 先根据烷烃的条件,确定烷烃的分子式,然后再根据官能团位置异构确定烯烃的同分异构体.
解答 解:第一步:确定该烷烃碳原子个数
①主链为4个碳原子的烷烃,其支链只能是甲基(不可能是乙基,否则主链超过4个碳原子).
②主链为4个碳原子的烷烃,支链数最多4个(下面的0,是指该物质只有一种,没有同分异构体)
甲基的个数 同分异构体
1个 0
2个 2
3个 0
4个 0
③结论:该烷烃总共有6个碳原子,
第二步:分析烯烃的同分异构体数目
①双键在1号位,有以下3种
C=C-C-C
1 2 3 4
2-乙基丁烯、2,3-二甲基丁烯、3,3-二甲基丁烯
②双键在2号位,有1种
C-C=C-C
1 2 3 4
2,3-二甲基-2-丁烯
结论:共有4种.
故选B.
点评 本题主要考查了同分异构体的写法,能熟练书写1-6个碳的碳链异构;常规的书写方法:碳链异构→位置异构→类别异构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8. 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
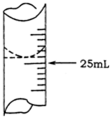
(1)若甲同学在实验过程中,记录滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则此时消耗HCl标准溶液的体积为23.80mL.
(2)乙学生做了2组平行实验,数据记录如下:
据此计算出待测NaOH溶液的物质的量浓度为0.0800 mol•L-1(小数点后保留四位);乙同学判断达到滴定终点时的现象为滴入最后一滴盐酸,溶液有红色变为无色,且半分钟不恢复红色.
 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol•L-1HCl标准溶液进行中和滴定(用酚酞作指示剂).请回答下列问题:(1)若甲同学在实验过程中,记录滴定前滴定管内液面读数为1.10mL,滴定后液面如图,则此时消耗HCl标准溶液的体积为23.80mL.
(2)乙学生做了2组平行实验,数据记录如下:
| 实验序号 | 待测NaOH溶液的体积/mL | HCl标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 20.10 |
| 2 | 25.00 | 1.50 | 21.40 |
6.下列分子中心原子均是sp2杂化的是( )
| A. | PBr3、NO2 | B. | CH4、SCl2 | C. | BF3、SO2 | D. | H2O、CS2 |
3.微量元素在人体内含量极少,但它们对于维持生命活动,促进人体健康生长和发育都有极其重要的作用.下列元素中,若缺乏严重会导致智力损害的是( )
| A. | 钙元素 | B. | 碘元素 | C. | 铁元素 | D. | 钠元素 |
19.用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“0”或“0”刻度线稍下,并记下读数;④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;⑤用标准液滴定至终点,记下滴定管液面读数.⑥重复以上滴定操作2-3次.请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果偏大 (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果无影响(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视锥形瓶中溶液颜色变化;判断到达滴定终点的依据是:锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(4)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是AB
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:0.1626mol/L.
①用蒸馏水洗涤碱式滴定管,注入0.2000mol/L的标准NaOH溶液至“0”刻度线以上;②固定好滴定管并使滴定管尖嘴充满液体;③调节液面至“0”或“0”刻度线稍下,并记下读数;④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;⑤用标准液滴定至终点,记下滴定管液面读数.⑥重复以上滴定操作2-3次.请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果偏大 (填“偏大”、“偏小”或“无影响”).
(2)步骤④中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果无影响(填“偏大”、“偏小”或“无影响”).
(3)步骤⑤滴定时眼睛应注视锥形瓶中溶液颜色变化;判断到达滴定终点的依据是:锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(4)以下是实验数据记录表
从表中可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是AB
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
| 滴定 次数 | 盐酸体积 (mL) | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5)根据表中记录数据,通过计算可得,该盐酸浓度为:0.1626mol/L.
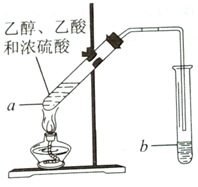 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了香味的酯.在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了香味的酯.在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.