题目内容
5.硒为第四周期VIA族元素,根据它在周期表中位置推测,硒不可能具有的性质( )| A. | 单质有还原性 | B. | 硒元素在化合物中可显-2价 | ||
| C. | 硒化氢水溶液显弱碱性 | D. | 最高价氧化物的水化物显酸性 |
分析 根据Se位于元素周期表中的第四周期第ⅥA族,硒与氧、硫同主族,性质与S类似,非金属性O>S>Se,非金属性越强,其氢化物越稳定,最高价氧化物的水化物的酸性越强,并利用类推法来解答.
解答 解:A、单质硫在反应中可作还原剂,同主族元素从上往下金属性增强,所以单质硒具有还原性,故A正确;
B、最外层6个电子,易得2个电子达8电子的稳定结构,所以硒元素在化合物中可显-2价,故B正确;
C、H2Se与H2S性质类似,H2S的水溶液显弱酸性,则硒化氢的水溶液显弱酸性,故C错误;
D、非金属性Br>Se>As,则最高价氧化物的水化物的酸性HBrO4>H2SeO4>H3AsO4,所以最高价氧化物的水化物显酸性,故D正确;
故选C.
点评 本题考查学生利用元素周期律来解答,明确同主族元素性质的相似性和递变性是解答本题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列说法正确的是( )
| A. | 需要加热的化学反应都是吸热反应 | |
| B. | 水力发电是将化学能转化为电能的过程 | |
| C. | 可以通过化学反应完成16O到18O的转变 | |
| D. | 生铁、不锈钢、青铜都属于合金 |
13.如图是常见四种有机物的比例模型示意图.下列说法正确的是( )
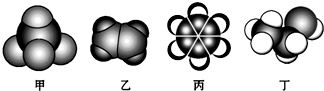

| A. | 甲中有少量乙杂质,可以通入到酸性高锰酸钾溶液中,洗气除杂 | |
| B. | 乙烷中有少量乙杂质,可以通入到溴水中,洗气除杂 | |
| C. | 丙中有少量苯酚杂质,可以先加浓溴水,然后静置,过滤除杂 | |
| D. | 丁有少量乙酸杂质,可以加少量浓硫酸并加热除杂 |
20.已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数c>d | B. | 非金属性Y<Z | ||
| C. | 氢化物的稳定性H2Y>HZ | D. | 原子半径W>X |
17.下列各项中正确的是( )
| A. | 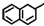 中所有碳原子可能在同一平面上 中所有碳原子可能在同一平面上 | |
| B. | 丙烷中所有的原子均在一个平面 | |
| C. | C4H8属于烯烃的同分异构体共有4种(含顺反异构) | |
| D. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 |
14.下列溶液中,能用带磨口玻璃塞的试剂瓶盛放的是( )
| A. | 浓硫酸 | B. | 水玻璃 | C. | 氢氟酸 | D. | 苛性钾溶液 |