题目内容
5. Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,其工作原理如图所示.电池总反应是:Mg+H2O2+2H+═Mg2++2H2O
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,其工作原理如图所示.电池总反应是:Mg+H2O2+2H+═Mg2++2H2O①负极材料为镁,发生氧化反应(填氧化或还原)
②两极电极反应式为:负极:Mg-2e-═Mg2+正极:H2O2+2H++2e-═2H2O.
③有4.8gMg反应时时,外电路中转移电子数为0.4NA.
分析 镁-H2O2酸性燃料电池中,镁为活泼金属,应为原电池的负极,被氧化,电极反应式为Mg-2e-═Mg2+,H2O2具有氧化性,应为原电池的正极,被还原,电极反应式为H2O2+2H++2e-═2H2O,据此分析解答.
解答 解:①镁-H2O2酸性燃料电池中,镁为活泼金属,应为原电池的负极发生氧化反应,则负极材料为镁,发生氧化反应,故答案为:镁;氧化;
②镁为活泼金属,应为原电池的负极,被氧化,电极反应式为Mg-2e-═Mg2+,H2O2具有氧化性,应为原电池的正极,被还原,电极反应式为H2O2+2H++2e-═2H2O,故答案为:Mg-2e-═Mg2+;H2O2+2H++2e-═2H2O;
③由负极电极反应式为Mg-2e-═Mg2+,则有4.8gMg反应时,外电路中转移电子数为$\frac{4.8g}{24g/mol}$×2=0.4NA;故答案为:0.4NA.
点评 本题考查原电池的知识,题目难度中等,注意过呢据物质的性质判断正负极反应以及电极反应式的书写,正确书写电极反应式为解答该题的关键,学习中注意体会书写方法.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
8.水杨酸、冬青油、阿司匹林的结构简式如图,下列说法不正确的是( )
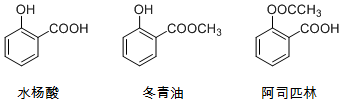

| A. | 由水杨酸制冬青油的反应是取代反应 | |
| B. | 阿司匹林的分子式为C9H8O4,水解可得水杨酸 | |
| C. | 冬青油苯环上的一氯取代物有4种 | |
| D. | 可用NaOH溶液除去冬青油中少量的水杨酸 |
16.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2+2H2O↑.下列有关该反应的说法正确的是( )
| A. | H2C2O4是氧化剂 | |
| B. | KClO3是还原剂 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应有2mol电子转移 |
20.NiCl2是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产NiCl2,继而生产Ni2O3的工艺流程如图:

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有:增大盐酸的浓度(或将镍废料研成粉末或延长浸泡时间等)(写出一种即可).
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 9.2 |
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
8.下列关于有机化合物的说法正确的是( )
| A. | 乙烯能够使溴水褪色,是因为乙烯和溴水反应生成了2-溴乙烷 | |
| B. | 将红热的铜丝插入到1-丙醇中,可以制得丙酮 | |
| C. | 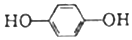 和苯酚互为同系物 和苯酚互为同系物 | |
| D. | 分子式为C10H12具有两个邻位链烃取代基的芳香烃有4种(不考虑立体异构) |
9.下列说法正确的是( )
| A. | 等质量的铝分别与足量Fe2O3或Fe3O4发生铝热反应时,转移电子的数目相等 | |
| B. | 质量分数分别为40%和60%的硫酸溶液等体积混合,所得溶液的质量分数为50% | |
| C. | 金属钠着火时,立即用泡沫灭火器灭火 | |
| D. | 洗涤做焰色反应的铂丝,可选用稀盐酸或稀硫酸 |
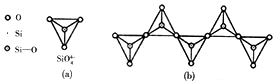

 3-甲基戊烷
3-甲基戊烷 2,2-二甲基-3-乙基戊烷.
2,2-二甲基-3-乙基戊烷.