题目内容
同位素示踪法是探究化学反应机理的重要方法,为了验证盐类水解的机理,现设计了两个对照实验,①NH4Cl溶于重水D2O,②将CH3COONa溶于重氧水(H218O),根据你学过的知识,你认为下列说法不正确的是( )
| A、两个示踪试验是为了说明盐类的水解是盐中的弱的离子与水电离出的H+或OH-结合形成弱电解质的过程 |
| B、实验①中,最终同位素D将存在于NH3?DHO、D2O、D+(或D3O+)中 |
| C、实验②中,水解的离子方程式可表示为:CH3COO-+2H218O?CH3COOH+18OH- |
| D、若将NH4Cl溶于H218O和D2O的混合水中,将得到ND3?H218O |
考点:探究化学反应机理,离子方程式的书写
专题:
分析:NH4Cl水解是NH4+结合水电离出的OH-,CH3COONa水解是CH3COO-结合水电离出的H+,根据盐的水解原理:弱离子结合水电离出来的氢离子或是氢氧根离子形成弱酸或是弱碱的过程来回答.
解答:
解:NH4Cl水解是NH4+结合水电离出的OH-,CH3COONa水解是CH3COO-结合水电离出的H+,
A、盐类的水解是盐中的弱的离子与水电离出的H+或OH-结合形成弱电解质的过程,两个对照实验能说明这一点,故A正确;
B、NH4Cl在D2O中水解是NH4+结合水电离出的OD-,即:NH4++D2O?NH3?DHO+D+,或DNH4++2D2O?NH3?DHO+D3O+,即同位素D将存在于NH3?DHO、D2O、D+(或D3O+),故B正确;
C、CH3COONa在重氧水(H218O)中水解是CH3COO-结合水电离出的H+,CH3COO-+2H218O?CH3COOH+18OH-,故C正确;
D、若将NH4Cl溶于H218O和D2O的混合水中,将得到NH3?DHO、NH3?H218O,故D错误.
故选D.
A、盐类的水解是盐中的弱的离子与水电离出的H+或OH-结合形成弱电解质的过程,两个对照实验能说明这一点,故A正确;
B、NH4Cl在D2O中水解是NH4+结合水电离出的OD-,即:NH4++D2O?NH3?DHO+D+,或DNH4++2D2O?NH3?DHO+D3O+,即同位素D将存在于NH3?DHO、D2O、D+(或D3O+),故B正确;
C、CH3COONa在重氧水(H218O)中水解是CH3COO-结合水电离出的H+,CH3COO-+2H218O?CH3COOH+18OH-,故C正确;
D、若将NH4Cl溶于H218O和D2O的混合水中,将得到NH3?DHO、NH3?H218O,故D错误.
故选D.
点评:本题考查学生盐的水解规律以及应用等知识,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、向饱和食盐水中先通足量CO2气体,再通入足量NH3,会析出NaHCO3晶体 |
| B、使用一定的催化剂可将汽车尾气中的CO和NO转化成CO2和N2 |
| C、将一定质量不同组成的铝钠合金投入足量盐酸中,铝的质量分数越小,放出的H2越多 |
| D、等质量的两份铝,分别和含n mol HCl和n mol NaOH 溶液反应,放出的气体的体积一定是NaOH溶液的多 |
警察常从案发现场的人体气味来获取有用线索,人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9?十一烷酸内酯;⑤十八烷;⑥己醛;⑦庚醛.下列说法正确的是( )
| A、①、②、⑥、⑦分子中碳原子数小于10 |
| B、①、②是无机物,③、⑤、⑦是有机物 |
| C、①是酸性化合物,②不是酸性化合物 |
| D、②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
下列有关说法正确的是( )
| A、李比希法、钠熔法、铜丝灼烧法等都是定量研究有机物中元素组成的方法 |
| B、元素分析仪可用于分析有机物中的元素组成 |
| C、“钠熔法”的变化过程中钠必定发生还原反应 |
| D、根据1H核磁共振谱就可以确定任何有机物分子的结构 |
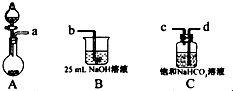 研究碳及其化合物的性质和用途是中学化学的任务之一.
研究碳及其化合物的性质和用途是中学化学的任务之一.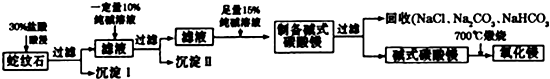
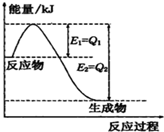 ①一定条件下,N2和H2反应生成lmolNH3过程中能量变化如图所示,则1mol N2完全反应时的焓变为:
①一定条件下,N2和H2反应生成lmolNH3过程中能量变化如图所示,则1mol N2完全反应时的焓变为: