题目内容
13.漂粉精的有效成分是次氯酸钙(写物质名称),工业上常用Cl2和Ca(OH)2(写化学式)反应制取漂粉精,其反应方程式可以表示为:2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.漂粉精露置在空气中容易变质失效,请用有关的反应方程式表示其原因:(1)Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO(2)2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
分析 氯气与石灰乳反应可制备,有效成分为次氯酸钙,漂粉精溶于水后,受空气中的CO2作用,生成次氯酸,次氯酸见光分解,从而变质,以此来解答.
解答 解:漂粉精的有效成分是Ca(ClO)2,名称为次氯酸钙,利用Cl2与Ca(OH)2制备,反应为2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,漂粉精露置在空气中容易变质失效,发生Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,
故答案为:次氯酸钙;Cl2;Ca(OH)2;2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O;Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
点评 本题考查漂白精,为高频考点,把握物质的性质、漂白原理为解答的关键,侧重分析与应用能力的考查,注意发生的反应,题目难度不大.

练习册系列答案
相关题目
3.已知常温下:Ksp(AgCl)=1.6×10-10,下列叙述正确的是( )
| A. | AgCl在饱和NaCl溶液中的Ksp比在纯水中的小 | |
| B. | AgCl的悬浊液中c(Cl-)=4×10-5.5mol/L | |
| C. | 将0.001 mol•L-1AgNO3溶液滴入0.001 mol•L-1的KCl,无沉淀析出 | |
| D. | 向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明Ksp(AgCl)<Ksp(AgBr) |
4.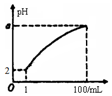 pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
 pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )| A. | a的取值范围为2<a<4 | |
| B. | HA溶液加热时,溶液酸性增强 | |
| C. | 与pH=12的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | HA溶液与NaOH溶液恰好完全反应时,c(Na+)>c(A-)>c(OH-)>c(H+) |
1.把任意比的NaHCO3和Na2O2的混合物放在密闭容器中加热.关于混合物加热前后消耗盐酸的物质的量,下列结论判断正确的是( )
| A. | 加热前后一样多 | B. | 加热前消耗的多 | ||
| C. | 加热后消耗的多 | D. | 当Na2O2适量时才会一样多无法 |
8.下列叙述正确的是( )
| A. | 用冰冷却苯,苯可以凝结成无色的晶体 | |
| B. | 苯与溴水混合后因发生反应而使溴水褪色 | |
| C. | 在苯中加入酸性 KMnO4 溶液,振荡后静置,上层液体为紫红色 | |
| D. | 1 mol 苯能与 3 mol H2发生加成反应,说明在苯环中含有 3 个双键 |
18.下列物质在水溶液中没有漂白作用的是( )
| A. | Cl2 和 NaClO | B. | Na2O2 和 H2O2 | C. | NaOH | D. | SO2和活性炭 |
3.化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )
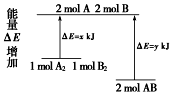

| A. | 该反应的反应热△H=x-y kJ/mol | |
| B. | 断裂1 mol A-A键和1 mol B-B键放出x kJ能量 | |
| C. | 2 mol AB的总能量高于1 mol A2和1 mol B2总能量 | |
| D. | 该反应是吸热反应 |

 25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示:
25℃时,向10mL 0.1mol•L-1 NH4HSO4溶液中逐滴滴入0.1mol•L-1 NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示: