题目内容
9.聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景. PPG的一种合成路线如下:
已知:
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃:化合物C的分子式为C5H8
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质
④R1CHO+R2CH2CHO$\stackrel{稀NaOH}{→}$

回答下列问题:
(1)A的结构简式为
 .
.(2)由B生成C的化学方8式为
 .
.(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛.
(4)①由D和H生成PPG的化学方程式为
 .
.②若PPG平均相对分子质量为10000,则其平均聚合度约为 (填标号).b
a. 48b. 58c. 76d.122
(5)D的网分异构体中能同时满足下列条件的共有5 种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体 ②既能发生银镜反应,又能发生皂化反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 (写姑构简式):

(6)D的所有同分异构体在下列-种表征仪器中显示的信号(或数据)完全相同,该仪器是c(填标号).
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪.
分析 烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为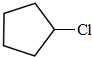 ,B发生消去反应生成C为
,B发生消去反应生成C为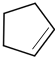 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(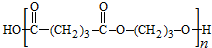 ),以此来解答.
),以此来解答.
解答 解:烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为 ,B发生消去反应生成C为
,B发生消去反应生成C为 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(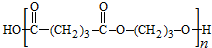 ),
),
(1)A的结构简式为 ,
,
故答案为: ;
;
(2)由B生成C的化学方程式为 ,
,
故答案为: ;
;
(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛,
故答案为:加成反应;3-羟基丙醛;
(4)①由D和H生成PPG的化学方程式为 ,
,
故答案为: ;
;
②若PPG平均相对分子质量为10000,则其平均聚合度约为$\frac{10000}{12×8+16×4+1×12}$≈58,
故答案为:b;
(5)D的同分异构体中能同时满足①能与饱和NaHCO3溶液反应产生气体,含-COOH,②既能发生银镜反应,又能发生水解反应-COOCH,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 ,故答案为:5;
,故答案为:5; ;
;
(6)D及同分异构体中元素组成相同,所以由元素分析仪显示的信号(或数据)完全相同,故选c.
点评 本题考查有机物的推断,为高频考点,为2015年高考真题,把握合成中碳链变化、官能团变化及反应条件推断物质为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案| A. | 标准状况下4.48L的二氧化碳 | |
| B. | 3.2g氧气(氧气的摩尔质量为32g.mol-1) | |
| C. | 含0.4NA个分子的氢气 | |
| D. | 0.5mol氮气 |
| 实验目的 | 试剂及方法 |
| 除去细沙中混有的碘 | A |
| 证明某些雨水样品呈酸性 | C |
| 鉴别甲烷和乙烯 | D |
| 除去开水壶内壁的水垢 | B |
B.加适量的食醋振荡
C.用pH试纸测定溶液pH
D.分别通入酸性高锰酸钾溶液.
| A. | 气态氢化物的稳定性:X<Z<W | |
| B. | X、Z、W氧化物对应水化物酸性的强弱顺序为X<Z<W | |
| C. | Y的阳离子半径比W的阴离子半径小 | |
| D. | 室温下,含Y元素的盐形成的水溶液其pH<7 |
| A. | 酒精、汽油都是有机溶剂,可以清洗衣服上的油污斑点 | |
| B. | 硫酸可以作铅蓄电池的电解质,也可用于溶解除去锅炉和水壶里的水垢 | |
| C. | 废旧塑料制品、废旧金属制品要回收和利用 | |
| D. | 推广太阳能、风能等新能源技术是施行低碳经济的有效途径 |
| A. | (1)(2) | B. | (3)(4) | C. | (1)(3) | D. | (2)(4) |
| A. | 已知:①2H2(g)+O2(g)═2H2O(g)△H1=-a kJ•mol-1, ②2H2(g)+O2(g)═2H2O(l)△H2=-b kJ•mol-1, 则a>b,△H1<△H2 | |
| B. | 同温同压下,SO2(g)+2CO(g)═2CO2(g)+S(l)在有无催化剂条件下的△H不同 | |
| C. | 任何酸与碱发生中和反应生成1mol H2O的过程中,能量变化均相同 | |
| D. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含2.0 g氢氧化钠的稀溶液与稀盐酸完全中和,放出热量2.865 kJ |

 合成氨工业的核心反应是N2(g)+3H2(g)?2NH3(g);反应过程中能量变化如图所示,回答下列问题.
合成氨工业的核心反应是N2(g)+3H2(g)?2NH3(g);反应过程中能量变化如图所示,回答下列问题.