题目内容
下列表达正确的是( )
A、NaCl的电子式: |
B、CO2的分子模型示意图: |
C、CrO5的结构式为: 该氧化物中Cr为+6价 该氧化物中Cr为+6价 |
| D、次氯酸的结构式:H-Cl-O |
考点:电子式,结构式,球棍模型与比例模型
专题:化学用语专题
分析:A.氯化钠为离子化合物,电子式中需要标出阴阳离子所带电荷;
B.二氧化碳为直线型结构,不是V型;
C.氧元素的化合价为-2价,根据氧元素化合价判断Cr的化合价;
D.次氯酸中不存在氢氯键,其分子中存在1个氧氢键和1个氧氯键.
B.二氧化碳为直线型结构,不是V型;
C.氧元素的化合价为-2价,根据氧元素化合价判断Cr的化合价;
D.次氯酸中不存在氢氯键,其分子中存在1个氧氢键和1个氧氯键.
解答:
解:A.氯化钠属于离子化合物,氯化钠的电子式中需要标出所得电荷,阴离子氯离子需要标出最外层电子,氯化钠正确的电子式为 ,故A错误;
,故A错误;
B.二氧化碳分子中存在两个碳氧双键,为直线型结构,二氧化碳的比例模型为 ,故B错误;
,故B错误;
C.CrO5的结构式为 ,该氧化物中氧元素化合价为-2、-1价,则Cr的化合价为+6价,故C正确;
,该氧化物中氧元素化合价为-2、-1价,则Cr的化合价为+6价,故C正确;
D.次氯酸的电子式为 ,将共用电子对换成短线即为结构式,次氯酸的结构式为H-O-Cl,故D错误;
,将共用电子对换成短线即为结构式,次氯酸的结构式为H-O-Cl,故D错误;
故选C.
 ,故A错误;
,故A错误;B.二氧化碳分子中存在两个碳氧双键,为直线型结构,二氧化碳的比例模型为
 ,故B错误;
,故B错误;C.CrO5的结构式为
 ,该氧化物中氧元素化合价为-2、-1价,则Cr的化合价为+6价,故C正确;
,该氧化物中氧元素化合价为-2、-1价,则Cr的化合价为+6价,故C正确;D.次氯酸的电子式为
 ,将共用电子对换成短线即为结构式,次氯酸的结构式为H-O-Cl,故D错误;
,将共用电子对换成短线即为结构式,次氯酸的结构式为H-O-Cl,故D错误;故选C.
点评:本题考查了电子式、结构式、比例模型等知识的判断,题目难度中等,注意掌握电子式、结构式、结构简式等化学用语的概念及判断方法,明确离子化合物与共价化合物的电子式的区别.

练习册系列答案
相关题目
下列说法正确的是( )
| A、1 mol物质的质量就是该物质的摩尔质量 |
| B、1 mol气体的体积就是气体摩尔体积 |
| C、1 mol任何粒子的相应粒子数叫做阿伏加德罗常数 |
| D、1 mol HCl溶于1 L水中,所得盐酸的物质的量浓度为1 mol?L-1 |
下列离子方程式不正确的是( )
| A、向100mL 0.1mol/L的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
| C、用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O═NaHCO3↓+NH4+ |
D、向水杨酸( )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: |
下列离子方程式书写正确的是( )
| A、澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2═CaCO3↓+H2O |
| B、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、二氧化硅与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| D、硅酸和烧碱溶液中和:H++OH-═H2O |
SO2的回收利用方案如图所示.下列说法错误的是( )
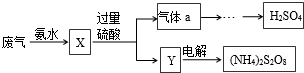

| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y中含NH4HSO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
 短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角.下列判断正确的是( )| A、离子半径:T<W<G |
| B、等物质的量的W、G单质分别与足量铁粉反应,后者消耗的铁粉多 |
| C、最简单气态氢化物的热稳定性:Q<R |
| D、T和G组成的化合物溶于水,其水溶液呈中性 |
在多电子原子中,轨道能量是由以下哪些因素决定( )
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子自旋状态.
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子自旋状态.
| A、①② | B、①④ | C、②③ | D、③④ |


