题目内容
16.以下判断中不正确的是( )| A. | 微粒半径:Fe2+>Fe3+ | |
| B. | 酸性:HClO4>H2SO4>H2SeO4 | |
| C. | 反应活泼性:O>03>02 | |
| D. | 物质的量浓度:pH相等时,CH3C00H>HCl0. |
分析 A.同种元素,失去电子少的半径大;
B.非金属性越强,最高价氧化物的酸性越强;
C.O原子易得到电子,臭氧的氧化性比氧气强;
D.醋酸的酸性强,HClO的酸性弱,等浓度时HClO的pH大.
解答 解:A.同种元素,失去电子少的半径大,则微粒半径:Fe2+>Fe3+,故A正确;
B.非金属性Cl>S>Se,最高价氧化物的酸性为HClO4>H2SO4>H2SeO4,故B正确;
C.O原子易得到电子,臭氧的氧化性比氧气强,则反应活泼性:O>03>02,故C正确;
D.醋酸的酸性强,HClO的酸性弱,等浓度时HClO的pH大,则pH相等时,浓度为CH3C00H<HCl0,故D错误;
故选D.
点评 本题考查周期表和周期律的综合应用,为高频考点,把握元素的性质、元素周期律、元素化合物知识为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.可逆反应:
(Ⅰ)2A(g)+B(g)?2C(g)+Q
(Ⅱ)3A(g)?D(g)+E(g)-Q,
下列条件均能使反应(Ⅰ)、(Ⅱ)中A的转化率增大的是( )
①增大压强 ②升高温度 ③增加A的浓度.
(Ⅰ)2A(g)+B(g)?2C(g)+Q
(Ⅱ)3A(g)?D(g)+E(g)-Q,
下列条件均能使反应(Ⅰ)、(Ⅱ)中A的转化率增大的是( )
①增大压强 ②升高温度 ③增加A的浓度.
| A. | 仅① | B. | ①③ | C. | ①②③ | D. | 都不能 |
7.下列物质不能通过化合反应得到的物质是( )
| A. | CuCl2 | B. | FeCl2 | C. | FeS | D. | CuS |
4.我国科学家不久前成功合成了3mm长的管状定向碳纳米管,长度居世界之首,这种碳纤维具有强度高、硬度(抵抗变形能力)高、密度小(只有钢的$\frac{1}{4}$)、熔点高、化学稳定性好等特点,因而被称为“超级纤维”.对碳纤维的下列说法中不正确的是( )
| A. | 它是制造飞机的理想材料 | B. | 它是一种新的碳单质 | ||
| C. | 它的结构与石墨相似 | D. | 碳纤维复合材料不易导电 |
11.为了提纯如表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | KMnO4酸性溶液 | 洗气 |
| B | 硝基苯(苯) | 水 | 分液 |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
3.下列物质中含有共价键的是( )
| A. | NaOH | B. | NaCl | C. | MgO | D. | Ne |
20.酸化是化学实验室中常用的操作之一,下列酸化处理正确的是( )
| A. | 检验CH3CH2Cl碱性水解产生的Cl-,先要用稀硫酸酸化,再检验 | |
| B. | KMnO4溶液通常可用盐酸酸化,以增强氧化性 | |
| C. | 配置Fe(NO3)2溶液时,用硝酸酸化,可抑制水解 | |
| D. | 鉴别溶液中是否有SO42-,先用盐酸酸化,再加BaCl2溶液 |
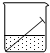
1.如图所示,将铁钉放入纯水中,一段时间后,铁钉表面有铁锈生成,下列说法正确的是( )

| A. | 铁钉与水面交接处最易腐蚀 | |
| B. | 铁钉发生吸氧腐蚀,铁做阴极 | |
| C. | 铁发生的反应是:Fe-3e→Fe3+ | |
| D. | 水上和水下部分的铁钉不发生电化腐蚀 |
 某种氢氧燃料电池的电解液为K0H溶液,该燃料电池的总反应方程式为:2H2+O2═2H2O.完成下列问题.
某种氢氧燃料电池的电解液为K0H溶液,该燃料电池的总反应方程式为:2H2+O2═2H2O.完成下列问题.