题目内容
8.若NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 1 mol Na2O2固体中含离子总数为4 NA | |
| B. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| C. | 常温下,pH=13的NaOH溶液中OH-离子数目为0.1 NA | |
| D. | 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,若反应放出9.2 kJ热量,则参加反应的氢分子数目为0.3 NA |
分析 A、过氧化钠由2个钠离子和1个过氧根构成;
B、求出混合物的物质的量,然后根据氢气和氮气均为双原子分子来分析;
C、溶液体积不明确;
D、反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出92KJ热量时,反应掉3mol氢气.
解答 解:A、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含3mol离子即3NA个,故A错误;
B、标况下22.4L混合物的物质的量为1mol,而氢气和氮气均为双原子分子,故1mol混合物中含2mol原子即2NA个,故B错误;
C、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故C错误;
D、反应3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol放出92KJ热量时,反应掉3mol氢气,故当放出9.2KJ时,参加反应的氢气为0.3mol,个数为0.3NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
3.下列现象或事实的解释正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 过氧化钠作呼吸面具中的供氧剂 | 过氧化钠将二氧化碳氧化成氧气 |
| B | 向Fe2(SO4)3溶液中加入铜粉,溶液变蓝色 | Cu2+的氧化性比Fe3+的弱 |
| C | 将表面有Ag2S的银首饰放在含食醋的铝锅中煮沸,首饰变得光亮 | 铝置换出银 |
| D | 向NaClO和NaOH混合溶液中加入H2O2浓溶液产生大量气体 | 碱性条件下,ClO-被还原为Cl2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有机物的命名正确的是( )
| A. | 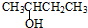 2-羟基丁烷 2-羟基丁烷 | B. |  :3-乙基-1-丁烯 :3-乙基-1-丁烯 | ||
| C. |  :1,3-二溴丙烷 :1,3-二溴丙烷 | D. | 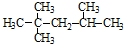 :2,2,3-三甲基戊烷 :2,2,3-三甲基戊烷 |
16.下列化学用语或模型表示正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | 氮气的电子式 | ||
| C. | 麦芽糖的化学式:C6H12O6 | D. | C2H4分子球棍模: |
3.中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )
| A. |  火法炼铜 | B. |  粘土制陶瓷 | C. |  树皮造纸 | D. |  打磨磁石制 |
20.下列叙述不正确的是( )
| A. | 锌跟稀硫酸反应制取氢气,加入少量的硫酸铜能加快反应速率 | |
| B. | 镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 | |
| C. | 钢铁表面常易被锈蚀生成Fe2O3•nH2O | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,电极反应相同的是负极反应 |
17.下列有关药品的处理中,正确的是( )
| A. | 取用药品时,不慎取多了,实验完毕将所剩药品放回原试剂瓶中 | |
| B. | 倾倒液体时,应注意标签要对着手心 | |
| C. | 实验室中含硫酸的废液可以直接倒入水槽,用水冲入下水道 | |
| D. | 取用金属钠时,能用手直接拿取 |
18.下列物质直接参与的反应与氧化还原反应无关的是( )
| A. | 维生素C用作贫血患者补铁剂的搭档 | |
| B. | 生石灰用作煤炭燃烧的固硫剂 | |
| C. | 氯化铁溶液用于腐蚀印刷电路板 | |
| D. | 高铁酸盐(Na2FeO4)用于饮用水的处理 |