题目内容
16.下列化学用语或模型表示正确的是( )| A. | HClO的结构式:H-Cl-O | B. | 氮气的电子式 | ||
| C. | 麦芽糖的化学式:C6H12O6 | D. | C2H4分子球棍模: |
分析 A、次氯酸的中心原子是氧原子,根据成键情况来书写结构式;
B、要将原子的最外层电子全部表示出来;
C、麦芽糖是二糖;
D、乙烯中碳原子间以双键相连.
解答 解:A、次氯酸的中心原子是氧原子,结构式为H-O-Cl,故A错误;
B、氮气中存在三对共用电子对,为三键,但每个氮原子还有两个孤对电子,故氮气的电子式为 ,故B错误;
,故B错误;
C、麦芽糖是二糖,和蔗糖互为同分异构体,化学式为:C12H22O11,故C错误;
D、乙烯中碳原子间以双键相连,氢原子分别连在碳原子上,故球棍模型为 ,故D正确.
,故D正确.
故选D.
点评 本题考查了有机物的结构式、分子式和电子式的书写等,难度不大,应注意的是次氯酸的结构式的书写.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A是原子半径最小的元素,A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍.下列叙述正确的是( )
| A. | 元素的原子半径:A<B<C<D<E | |
| B. | 对应氢化物的热稳定性:D>E | |
| C. | B与C、B与D形成的化合物中化学键类型相同 | |
| D. | 五种元素中最高价氧化物对应的水化物酸性最强的是E |
7.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: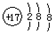 | |
| B. | 乙烯的结构简式为CH2CH2 | |
| C. | 氯化镁的电子式: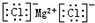 | |
| D. | 硫酸的电离方程式:H2SO4═H2++SO42ˉ |
4.下列有关物质性质的应用正确的是( )
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| B. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| C. | 生石灰能与水反应,可用来干燥氯气 | |
| D. | 二氧化硅不与强酸反应,可用石英作为反应容器制取氢氟酸 |
1.某有机物在氧气中充分燃烧,生成等物质的量的水和二氧化碳,则该有机物必须满足的条件是( )
| A. | 分子中的C、H、O的个数比为1:2:1 | B. | 分子中C、H个数比为1:2 | ||
| C. | 该有机物的相对分子质量为14 | D. | 该分子中肯定不含氧元素 |
8.若NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1 mol Na2O2固体中含离子总数为4 NA | |
| B. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| C. | 常温下,pH=13的NaOH溶液中OH-离子数目为0.1 NA | |
| D. | 3H2(g)+N2(g)?2NH3(g)△H=-92 kJ/mol,若反应放出9.2 kJ热量,则参加反应的氢分子数目为0.3 NA |
5.由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化 3MnO2+KClO3+6KOH $\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化 3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
完成下列填空:
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.泥三角
(2)在“加酸岐化”时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
反应之后得到高锰酸钾的步骤是:过滤、蒸发结晶、趁热过滤.
该步骤能够得到高锰酸钾的原理是KMnO4和K2CO3的溶解度不同.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$ 2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为 K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
熔融氧化 3MnO2+KClO3+6KOH $\stackrel{高温}{→}$3K2MnO4+KCl+3H2O
加酸歧化 3K2MnO4+2CO2→2KMnO4+MnO2↓+2K2CO3
已知相关物质的溶解度(20℃)
| 物质 | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度g/100g | 111 | 33.7 | 11.1 | 6.34 |
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd.(填序号)
a.瓷坩埚 b.蒸发皿 c.铁坩埚 d.泥三角
(2)在“加酸岐化”时不宜用硫酸的原因是生成K2SO4溶解度小,会降低产品的纯度;不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量.
反应之后得到高锰酸钾的步骤是:过滤、蒸发结晶、趁热过滤.
该步骤能够得到高锰酸钾的原理是KMnO4和K2CO3的溶解度不同.
(3)采用电解法也可实现K2MnO4的转化,2K2MnO4+2H2O$\stackrel{通电}{→}$ 2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为 K2MnO4中的锰元素可以完全转化到KMnO4中,原子利用率高.
6.下列试剂的保存方法错误的是( )
| A. | 少量的钠保存在煤油中 | B. | 漂白粉密封保存 | ||
| C. | 新制的氯水保存在棕色玻璃瓶中 | D. | 少量的钠保存在四氯化碳中 |
