题目内容
已知A和B两支试管的溶液中共含有K+、Ag+、Mg2+、Cl-、OH-、NO3-六种离子,向试管A中滴入酚酞试液呈红色.请回答下列问题:
(1)试管A的溶液中含有上述离子中的 ;
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为 (填A或B);
(3)若向试管B的溶液中加入合适的药品,过滤后可以回收一种金属和仅含一种溶质的溶液,则加入的药品是 (填化学式),涉及的离子方程式为 ;
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,该纯净物的名称为 ,混合过程中涉及的离子方程式为 .
(1)试管A的溶液中含有上述离子中的
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以回收一种金属和仅含一种溶质的溶液,则加入的药品是
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,该纯净物的名称为
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:试管A的溶液中滴入酚酞试液呈粉红色,说明溶液显碱性,一定含有OH-,根据离子共存原理,一定没有Ag+、Mg2+,一定含有K+.试管B中一定含有Ag+、Mg2+,则一定没有Cl-,一定含有NO3-;
(1)根据以上分析判断试管A的溶液中存在的离子;
(2)根据试管A和B中含有的离子进行分析;
(3)根据过滤后溶液中仅含有一种溶质,且得到相应的金属进行分析;
(4)根据A、B溶液中存在的离子形成反应的离子方程式.
(1)根据以上分析判断试管A的溶液中存在的离子;
(2)根据试管A和B中含有的离子进行分析;
(3)根据过滤后溶液中仅含有一种溶质,且得到相应的金属进行分析;
(4)根据A、B溶液中存在的离子形成反应的离子方程式.
解答:
解:向试管A的溶液中滴入酚酞试液呈粉红色,说明溶液显碱性,一定含有OH-,根据离子共存原理,一定没有Ag+、Mg2+,一定含有K+.试管B中一定含有Ag+、Mg2+,则一定没有Cl-,一定含有NO3-;
综上所述,试管A中含有K+、OH-、Cl-,试管B中含有Ag+、Mg2+、NO3-,
(1)试管A的溶液中含有K+、OH-、Cl-,
故答案为:K+、OH-、Cl-;
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管中含有Ag+,为试管B,
故答案为:B;
(3)若向试管B的溶液中加入合适的药品后,过滤后溶液中仅含有一种溶质,且得到相应的金属,应该发生置换反应,且不引入其他离子,则加入药品是Mg,反应的离子方程式为:Mg+2Ag+=2Ag+Mg2+;
故答案为:Mg;Mg+2Ag+=2Ag+Mg2+;
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则Ag+与Cl-恰好完全反应,Mg2+和OH-恰好完全反应,剩余钾离子和硝酸根离子,混合过程中发生反应的离子方程式为:Ag ++Cl-=AgCl↓、Mg2++2OH-=Mg(OH)2↓,
故答案为:硝酸钾;Ag ++Cl-=AgCl↓、Mg2++2OH-=Mg(OH)2↓.
综上所述,试管A中含有K+、OH-、Cl-,试管B中含有Ag+、Mg2+、NO3-,
(1)试管A的溶液中含有K+、OH-、Cl-,
故答案为:K+、OH-、Cl-;
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管中含有Ag+,为试管B,
故答案为:B;
(3)若向试管B的溶液中加入合适的药品后,过滤后溶液中仅含有一种溶质,且得到相应的金属,应该发生置换反应,且不引入其他离子,则加入药品是Mg,反应的离子方程式为:Mg+2Ag+=2Ag+Mg2+;
故答案为:Mg;Mg+2Ag+=2Ag+Mg2+;
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则Ag+与Cl-恰好完全反应,Mg2+和OH-恰好完全反应,剩余钾离子和硝酸根离子,混合过程中发生反应的离子方程式为:Ag ++Cl-=AgCl↓、Mg2++2OH-=Mg(OH)2↓,
故答案为:硝酸钾;Ag ++Cl-=AgCl↓、Mg2++2OH-=Mg(OH)2↓.
点评:本题考查了离子共存及离子方程式的书写,题目难度中等,试题涉及的内容较多,充分考查了学生对所学知识的掌握情况;注意掌握离子反应发生的条件及离子方程式的书写方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

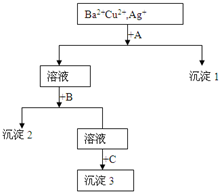 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图所示
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如图所示
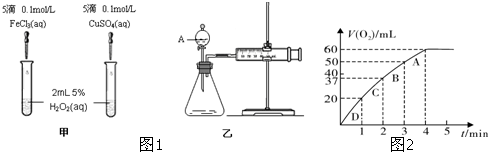
 已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-187.4kJ/mol.3000C时的恒容密闭容器中,当C(CO2)=1.00mol.L-1C(H2)=1.60mol.L-1开始反应,结果如图所示,回答下列问题:
已知CO2可以生产绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-187.4kJ/mol.3000C时的恒容密闭容器中,当C(CO2)=1.00mol.L-1C(H2)=1.60mol.L-1开始反应,结果如图所示,回答下列问题: