��Ŀ����
̼�����ڹ�ҵ���ж�����;�����罹̿��������ȡˮú����ұ������������̿�ɴ���������Ⱦ��NO��
һ�������£���2 L�ܱ������м���NO�ͻ���̿�������ʣ���Ӧ��������A��B�����¶���T1��ʱ����ø�����ƽ��ʱ���ʵ������±���
| | ����̿ (mol) | NO (mol) | A (mol) | B (mol) |
| ��ʼ | 2.030 | 0.100 | 0 | 0 |
| ƽ�� | 2.000 | 0.040 | 0.030 | 0.030 |
��1����T1��ʱ���ﵽƽ���ʱ2���ӣ���NO��ƽ����Ӧ����Ϊ mol��(L��min)��������̿����0.015molʱ����Ӧ��ʱ�� ������ڡ�����С�ڡ����ڡ���1���ӡ�
��2����T1���·�Ӧ�ﵽƽ������д�ʩ���ܸı�NO��ת���ʵ��� ��
a���������̿���� b������ѹǿ c�������¶� d����ȥ����B
��3������ϱ����ݣ��÷�Ӧ��ƽ�ⳣ������ʽΪ ����������A��B����Ӧ�Ļ�ѧʽ��ʾ����T1��ʱ��ƽ�ⳣ��ΪK1��T2��ʱ��ƽ�ⳣ��ΪK2����K1>K2���ܷ��жϸ÷�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ��˵���� ��
��1��0.015mol/(L��min)��С�ڣ�3�֣�
��2��a b��2�֣�
��3�� ��1�֣� ���ܣ���ȷ��T1��T2����Ըߵ͡������ܣ���T1>T2ʱ����Ӧ�����ȷ�Ӧ����T1<T2ʱ����Ӧ�Ƿ��ȷ�Ӧ��2�֣�
��1�֣� ���ܣ���ȷ��T1��T2����Ըߵ͡������ܣ���T1>T2ʱ����Ӧ�����ȷ�Ӧ����T1<T2ʱ����Ӧ�Ƿ��ȷ�Ӧ��2�֣�
�������������
��1���÷�ӦΪ�� C + 2NO = CO2 + N2
��ʼ�� 2.030 0.100 0 0
ƽ���� 2.000 0.040 0.030 0.030
NO����Ϊ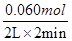 =0.015mol/(L��min)����Ӧ����������Ũ�ȵļ�С����С���ʿ�ʼ�죬ʱ��С��1min��
=0.015mol/(L��min)����Ӧ����������Ũ�ȵļ�С����С���ʿ�ʼ�죬ʱ��С��1min��
��2��a��CΪ���壬�ı���������ʹ��ѧƽ���ƶ���b������ѹǿƽ�⳯�����С�ķ����ƶ���������ת��������c���ı��¶ȣ�ƽ���ƶ���ת���ʸı䣻d����С������Ũ�ȣ�ƽ�������ƶ������Ըı�ת���ʡ�
��3������K�仯������ƽ���ƶ��������¶ȵı仯�������е����Ȼ��Ƿ��ȡ�
���㣺��ѧ��Ӧ���ʼ���ѧƽ���ƶ�����ѧƽ�ⳣ������ѧ��Ӧ������ؼ��㡣

 �¿α�������������ҵ�������γ�����ϵ�д�
�¿α�������������ҵ�������γ�����ϵ�д������°������·������ʵ�顣
| ʵ���� | ��Ӧ�� | ���� |
| �� | 10mL2% H2O2��Һ | �� |
| �� | 10mL5% H2O2��Һ | �� |
| �� | 10mL5% H2O2��Һ | 1mL0.1mol��L��1FeCl3��Һ |
| �� | 10mL5% H2O2��Һ������HCl��Һ | 1mL0.1mol��L��1FeCl3��Һ |
| �� | 10mL5% H2O2��Һ������NaOH��Һ | 1mL0.1mol��L��1FeCl3��Һ |
��1�������ܼӿ컯ѧ��Ӧ���ʵ�ԭ����_____________________________________��
��2��ʵ��ٺ͢ڵ�Ŀ����____________________________��ʵ��ʱ���ڽϳ�ʱ��û�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ���____________________��
��3��д��ʵ��۵Ļ�ѧ��Ӧ����ʽ ��
��4��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ����ͼ��
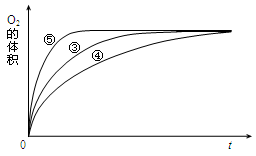
������ͼ�ܹ��ó���ʵ�������______________________________________��
��1��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g�� 2NH3��g�� ��H=��92.4 kJ/mol
2NH3��g�� ��H=��92.4 kJ/mol
���ڸ��¶�ʱ��ȡl mol N2��3 mol H2�����ܱ������У��ڴ��������½��з�Ӧ����÷�Ӧ�ų�����������_______92.4 kJ��(�С�ڡ��� �����ڡ� ���ڡ�)
��һ�������£��������淴Ӧ������̶����ܱ������н��У�����������˵����Ӧ�Ѵﵽƽ�����_______________��
| A��NH3���ɵ�������NH3�ֽ��������� |
B���������ķ�Ӧ���� v����NH3��=v����H2�� v����NH3��=v����H2�� |
| C�������ڵ��ܶȲ��ٱ仯 |
| D����λʱ��������a mol N2��ͬʱ����2a mol NH3 |
 ֵ��_____(����� ����С�� ���䡱)��
ֵ��_____(����� ����С�� ���䡱)����3�������£���0.001mol/LAlCl3��Һ��ͨ��NH3ֱ����������PH=_________ʱ����ʼ���ɳ���(��֪��Ksp[Al(OH)3]=1.0��10-33)
(14��)��ҵ���������Ҫ��Ӧ��4NH3(g)+5O2(g)  4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
4NO(g)+6H2O(g)��H=-akJ/mol(a��0)
(1)�����4molNH3��5molO2���������У��ﵽƽ��ʱ���ų�����0.8akJ����Ӧʱת�Ƶĵ�����Ϊ
mol
(2)�������������䣬���й�ϵͼ�д������ ��ѡ����ţ�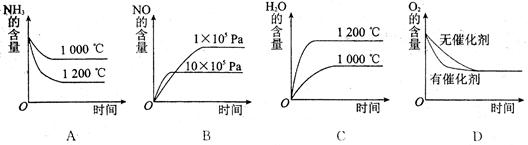
(3)t��ʱ�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�����±�
| Ũ��(mol/L) ʱ��(min) | c(NH3) | c(O2) | c(NO) | c(H2O) |
| �� ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | x | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�ٷ�Ӧ�ڵ�2mim����4mimʱ����Ӧ����v(O2)=
�ڵ�2minʱ�ı����������ı������������
A�������¶� B��ʹ���˴��� C����Сѹǿ D��������������
������ͬ���¶��£���ʼ�������м���NH3��O2��NO��H2O(g)��Ũ�ȶ�Ϊ1mol/L����÷�Ӧ���� _______�������(�����Ӧ��.���淴Ӧ��.�����ƶ���)
��4����ҵ����ˮ���ն��������������ᣬ���ɵ�NO2���徭��������������յ�ѭ������ʹ����ת��Ϊ���ᣨ�ٶ�������������������ʧ��������23��NO2����2���������յõ�20�G��ϡ���� �֡�
��5����Ʒ�����Ũ��Ϊ60%��70%��Ϊ����Ũ���ᣬ����Mg(NO3)2����ˮ����Ȼ�����������CaCl2��MgCl2����ˮ����ԭ����__________________________________________
��14�֣���ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
��1���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ�__________
| A������CH3OH������������CO��������� | B�����������ܶȲ��� |
| C�������������ƽ�������������� | D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯 |
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�ٸ÷�Ӧ��ѧƽ�ⳣ������ʽK=
���ɱ��������жϸ÷�Ӧ�ġ�H__________0���>������=����<������
��ij�¶��£���2molCO��6mol H2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���C(CO)=0.2mol��L-1����ʱ���¶�Ϊ__________
��3��25��101KPa�£�1gҺ̬�״���ȫȼ������CO2��Һ̬ˮʱ�ų�����22.68kJ����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ
��4���ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�ʮ�����õ�ع���ʱ�����缫��ӦʽΪ ������Ӧʱ����16g�״��������ĵ��ܵ��������CuSO4��Һ��������״���µ�O2________��
 cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ��
cC��g������H��0���ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯����������ͼ��ʾ�� 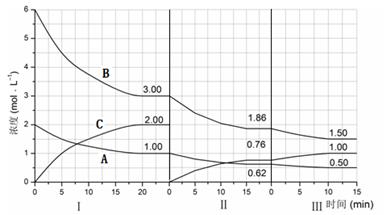


 2B(s) + 6HBr(g) ����ȡ���������������գ�
2B(s) + 6HBr(g) ����ȡ���������������գ�