题目内容
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下: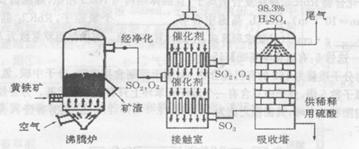
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在______的郊区(填标号)
A.有丰富黄铁矿资源的城市 B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市 D.人口稠密的文化、商业中心城市
(2)沸腾炉中发生反应的化学方程式为_____,接触室中发生反应的化学方程式是_____。
(3) 在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是_____。
A. 硫铁矿燃烧前要粉碎,因为大块的黄铁矿不能在空气中反应
B. 从沸腾炉出来的气体要净化,因为炉气中的SO2会与杂质反应
C. SO2氧化成SO3要用催化剂,这样可提高SO2的转化率
D. SO3用98. 3%的浓硫酸来吸收,目的是为了防止形成酸雾,以提髙SO3吸收效率
(4) 下表是压强对SO2平衡转化率的影响
对于SO2转化SO3的反应,增大压强可使转化率______________,但在实际工业生产中常采用常压条件,理由是________________________________。
(5)某工厂用500t含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是_____t。
(15分) (1)C (2分)
(2)4FeS2+11O2 2Fe2O3+8SO2 (2分) 2SO2+O2
2Fe2O3+8SO2 (2分) 2SO2+O2 2SO3 (2分)
2SO3 (2分)
(3)D (2分) (4)升高 常压下转化率已经很高,增加压强可提高转化率,但增加了设备、动力成本等,效益反而下降 (3分) (5)376.32t (4分)
解析试题分析:(1)A、硫酸厂厂址的选择综合经济效益考虑,硫酸产品的运输成本要高于原料黄铁矿的运输成本,故A不正确;B、风光秀丽的旅游城市,不靠近原料基地,也不靠近消耗硫酸的工业城市,导致原料运输与产品运输成本高,同时还会对旅游城市造成污染,故B不正确;C、由于硫酸产品的运输成本要高于原料黄铁矿的运输成本,所以厂址应选择在消耗硫酸甚多的工业城市,故C正确;D、人口稠密的文化、商业中心城市,远离原料基地和消耗硫酸的工业城市,同时为了防止污染环境,不宜考虑作为硫酸厂厂址.故D不正确,所以答案选C。
(2)黄铁矿在沸腾炉中发生反应,所以沸腾炉中发生反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2;生成的SO2在接触室中被氧化生成三氧化硫,因此接触室中发生反应的化学方程式是2SO2+O2
2Fe2O3+8SO2;生成的SO2在接触室中被氧化生成三氧化硫,因此接触室中发生反应的化学方程式是2SO2+O2 2SO3。
2SO3。
(3)A、在硫酸工业制法中,黄铁矿燃烧前需要粉碎,是为了增大与空气的接触面,加快反应速率,不是因为大块的黄铁矿不能在空气中燃烧,故A不正确;B、从沸腾炉出来的炉气中含有SO2、O2、N2、水蒸气、灰尘、砷硒化合物等,由于砷硒化合物能导致催化剂失去催化活性,因此需净化,不是因为炉气中二氧化硫会与杂质反应,故B不正确;C、二氧化硫氧化为三氧化硫时需使用催化剂,目的是加快反应速率,提高产量.并不能提高二氧化硫的转化率,故C不正确;D、在吸收塔中三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率.故D正确,答案选D。
(4)根据表中数据可知,增大压强,SO2的转化率升高。由于在常压下SO2转化率已经很高,增加压强可提高转化率,但增加了设备、动力成本等,效益反而下降,所以在实际工业生产中常采用常压条件。
(5)根据S元素守恒可知: FeS2~~~~~~~~~~~~~2H2SO4
120t 2×98t
500t×0.48×0.98×0.96 m×0.98
解得m=376.32t
考点:考查工业生产浓硫酸的有关判断、计算以及外界条件对反应速率和平衡状态的影响等

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案煤的液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,其中合成CH3OH是最重要的研究方向之一。在2L的密闭容器中,由CO2和H2合成甲醇CO2(g)+3H2(g) CH3OH(g)+H2O(g),在其他条件不变的情况下,探究温度对反应的影响,实验结果如下图所示(注:T2>T1均大于300℃)。
CH3OH(g)+H2O(g),在其他条件不变的情况下,探究温度对反应的影响,实验结果如下图所示(注:T2>T1均大于300℃)。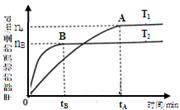
①通过分析上图,可以得出对反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)的说法正确的是(填
CH3OH(g)+H2O(g)的说法正确的是(填
序号) 。
| A.该反应为放热反应 |
| B.T1时的反应速率大于T2时的反应速率 |
| C.该反应在T1时的平衡常数比T2时的大 |
| D.处于A点的反应体系从T1变到T2,达平衡时n(H2)/n(CH3OH)增大 |
a.体系压强保持不变 b.v(H2)=3v(CO2)
c.CH3OH与H2物质的量之比为1:3 d.每消耗1 mol CO2的同时生成3molH2
e.密闭容器中混合气体的密度不变 f.密闭容器中CH3OH的体积分数不变
③在T1温度时,将2molCO2和6molH2充入该密闭容器中,充分反应达平衡时,若CO2的转化率为60%,则容器内的压强与起始压强之比为 ,该反应的平衡常数为 。
碳单质在工业上有多种用途。例如焦炭可用来制取水煤气、冶炼金属,活性炭可处理大气污染物NO。
一定条件下,在2 L密闭容器中加入NO和活性炭(无杂质)反应生成气体A和B。当温度在T1℃时,测得各物质平衡时物质的量如下表:
| | 活性炭 (mol) | NO (mol) | A (mol) | B (mol) |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| 平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)在T1℃时,达到平衡共耗时2分钟,则NO的平均反应速率为 mol/(L·min);当活性炭消耗0.015mol时,反应的时间 (填“大于”、“小于”或“等于”)1分钟。
(2)在T1℃下反应达到平衡后,下列措施不能改变NO的转化率的是 。
a.增大活性炭的量 b.增大压强 c.升高温度 d.移去部分B
(3)结合上表数据,该反应的平衡常数表达式为 。(生成物A、B用相应的化学式表示)若T1℃时的平衡常数为K1,T2℃时的平衡常数为K2,且K1>K2,能否判断该反应是吸热反应还是放热反应,说明理 。
 CO2(g)十H2 (g) △H<0 , CO和H2O浓度变化如下图,
CO2(g)十H2 (g) △H<0 , CO和H2O浓度变化如下图,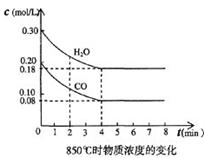
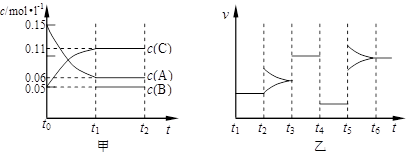
 2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):
2NH3(g)反应的影响,实验结果可表示成如图所示的规律(图中T表示温度,n表示物质的量):
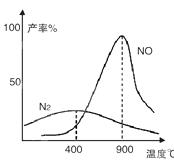
 4NO+6H2O ,4NH3+3O2
4NO+6H2O ,4NH3+3O2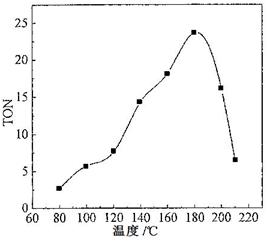
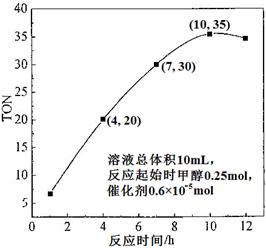
 NH3(g) + HI(g)
NH3(g) + HI(g)
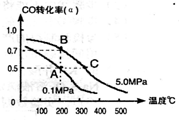
 CH3OH(g)+H2O(g)△H<0,若将6mo1 CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。
CH3OH(g)+H2O(g)△H<0,若将6mo1 CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如右图所示(实线)。
