题目内容
在如图所示的两个电化学装置中,连接灵敏电流计的并接通电路,两个电流计的指针均明显 偏转,下列说法错误的是( )
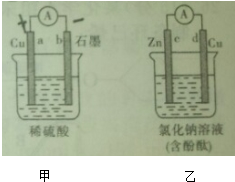

| A、甲溶液中H+的移动方向是a→b |
| B、b电极上的电极反应式为:2H++2e-═H2↑ |
| C、一段时间后,d电极附近的溶液变红 |
| D、乙装置中的溶液会逐渐变浑浊 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、甲溶液中a是活泼的电极发生氧化反应,作负极,b为正极,所以H+离子移动的方向为a→b;
B、电极上的电极反应式为:O2+4H++4e-═2H2O;
C、乙装置中发生吸氧腐蚀;
D、c极锌离子放电生成的锌离子与d极氧气放电产生的氢氧根离子结合成氢氧化锌浑浊.
B、电极上的电极反应式为:O2+4H++4e-═2H2O;
C、乙装置中发生吸氧腐蚀;
D、c极锌离子放电生成的锌离子与d极氧气放电产生的氢氧根离子结合成氢氧化锌浑浊.
解答:
解:A、甲溶液中a是活泼的电极发生氧化反应,作负极,b为正极,所以H+离子移动的方向为a→b,故A正确;
B、电极上的电极反应式为:O2+4H++4e-═2H2O,故B错误;
C、乙装置中发生吸氧腐蚀,电极反应式为:O2+2H2O-4e-═4OH-,所以d电极附近的溶液变红,故C正确;
D、c极锌离子放电生成的锌离子与d极氧气放电产生的氢氧根离子结合成氢氧化锌浑浊,故D正确;
故选B.
B、电极上的电极反应式为:O2+4H++4e-═2H2O,故B错误;
C、乙装置中发生吸氧腐蚀,电极反应式为:O2+2H2O-4e-═4OH-,所以d电极附近的溶液变红,故C正确;
D、c极锌离子放电生成的锌离子与d极氧气放电产生的氢氧根离子结合成氢氧化锌浑浊,故D正确;
故选B.
点评:本题考查电化学的相关知识,学生只要掌握原电池的反应原理就可以迅速解题,比较容易.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
| A、无水硫酸铜、蔗糖 |
| B、硅胶(具有吸湿性)、硫酸亚铁 |
| C、食盐、硫酸亚铁 |
| D、生石灰、食盐 |
下列关于化合价的说法正确的是( )
| A、在Na2O中,钠原子显+1价,氧原子显-2价 |
| B、在O2中,氧元素显-2价 |
| C、非金属元素在化合物中总显负价 |
| D、一种元素在同一种化合物中,可能有几种化合价 |
已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10 分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2 NaCN+HF=HCN+NaF NaNO2+HF=HNO2+NaF由此可判断下列叙述不正确的是( )
| A、K(HF)=7.2×10-4 |
| B、K(HNO2)=4.9×10-10 |
| C、根据两个反应即可得出结论 |
| D、Ka(HCN)<Ka(HNO2 ) |
如图所示,a、b两电极材料分别为铁棒和铜棒,则下列说法中不正确的是( )


| A、该装置可以构成原电池,也可构成电解池 |
| B、a极可能发生反应:Cu2++2e-═Cu |
| C、b电极质量可能增加 |
| D、该过程可能有大量气体产生 |
下列有关说法正确的是( )
| A、在轮船表面涂刷富锌油漆,能有效防止船体在海水中被腐蚀 | ||||
B、0.1 mol?L-1氨水加水稀释后,溶液中
| ||||
| C、用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 | ||||
| D、反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |