题目内容
如图所示,a、b两电极材料分别为铁棒和铜棒,则下列说法中不正确的是( )


| A、该装置可以构成原电池,也可构成电解池 |
| B、a极可能发生反应:Cu2++2e-═Cu |
| C、b电极质量可能增加 |
| D、该过程可能有大量气体产生 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池反应时,a极:Fe-2e-=Fe2+,b极:Cu2++2e-=Cu,a极发生氧化反应,b极发生还原反应,则该装置可能为原电池或电解池,利用化合价的变化来分析电极反应,以此来解答.
解答:
解:A.由图可知,该装置可能有外加电源,则可能为电解池,故A正确;
B.若装置为电解池,且a为阴极时,a、b两电极的反应式分别为Cu2++2e-═Cu、Cu-2e-═Cu2+,故B正确;
C.该装置为原电池时,b的电极反应式为:Cu2++2e-═Cu,所以b电极质量可能增加,故C正确;
D.若装置为原电池,则a、b两电极的反应式分别为Fe-2e-═Fe2+、Cu2++2e-═Cu,b极质量增加;若装置为电解池,且a为阴极时,a、b两电极的反应式分别为Cu2++2e-═Cu、Cu-2e-═Cu2+,故D错误;
故选D.
B.若装置为电解池,且a为阴极时,a、b两电极的反应式分别为Cu2++2e-═Cu、Cu-2e-═Cu2+,故B正确;
C.该装置为原电池时,b的电极反应式为:Cu2++2e-═Cu,所以b电极质量可能增加,故C正确;
D.若装置为原电池,则a、b两电极的反应式分别为Fe-2e-═Fe2+、Cu2++2e-═Cu,b极质量增加;若装置为电解池,且a为阴极时,a、b两电极的反应式分别为Cu2++2e-═Cu、Cu-2e-═Cu2+,故D错误;
故选D.
点评:本题考查原电池和电解池,利用氧化还原反应来分析电极反应是解答本题的关键,并熟悉工作原理来解答,难度不大.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
下列对氧化还原反应的分析中合理的是( )
| A、Mg变为MgO时化合价升高,因此,Mg在该反应中作还原剂 | ||||
| B、KMnO4受热分解时,Mn元素化合价一方面升高一方面降低,因此,在该反应中Mn元素既被氧化又被还原 | ||||
| C、凡是氧化还原反应都能造福人类 | ||||
D、在反应2H2O
|
下列说法中正确的是( )
| A、在一定温度和压强下,各种气态物质体积大小由构成气体分子大小决定 |
| B、在一定温度和压强下,各种气态物质体积的大小由构成气体的分子数决定 |
| C、不同的气体,若体积不同,则它们所含的分子数一定不同 |
| D、气体摩尔体积是指1mol任何气体所占的体积约为22.4L. |
已知25℃时有关弱酸的电离平衡常数如下表:下列推断正确的是( )
| 弱酸化学式 | HF | CH3COOH | HClO | H2CO3 |
| 电离常数 | 6.8×10-4 | 1.7×10-5 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
| A、弱酸的酸性强弱:HF<HClO |
| B、同物质的量浓度NaClO与NaHCO3溶液,前者的pH较大 |
| C、将碳酸钠粉末加入到0.1mol?L_1 HClO溶液中,不发生反应 |
| D、中和等体积、等pH的HF和CH3COOH溶液,消耗等量的NaOH |
在如图所示的两个电化学装置中,连接灵敏电流计的并接通电路,两个电流计的指针均明显 偏转,下列说法错误的是( )
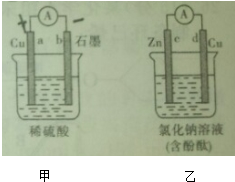

| A、甲溶液中H+的移动方向是a→b |
| B、b电极上的电极反应式为:2H++2e-═H2↑ |
| C、一段时间后,d电极附近的溶液变红 |
| D、乙装置中的溶液会逐渐变浑浊 |
以NA代表阿伏罗德常数,则下列关于热化学方程式:
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l);△H=-1300kJ?mol-1的说法正确的是( )
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l);△H=-1300kJ?mol-1的说法正确的是( )
| A、有10NA个电子转移时,该反应吸收1300kJ的能量 |
| B、有NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C、有2NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D、有8NA个碳氧共用电子对生成时,放出1300kJ的能量 |
 纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O
纳米级Cu2O由于具有优良的催化性能而受到关注.采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O
| ||
| A、钛电极发生氧化反应 |
| B、阳极附近溶液的pH逐渐增大 |
| C、离子交换膜应采用阳离子交换膜 |
| D、阳极反应式是:2Cu+2OH一一2e一═Cu2O+H2O |
向0.1mol/LCH3COOH溶液中加人CH3COONa晶体或加等体积水稀释时.都会引起( )
| A、溶液的pH增大 |
| B、CH3COOH的电离程度增大 |
| C、溶液的导电能力减弱 |
| D、溶液的c(OH-)减小 |