题目内容
8.有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl ⑧Ne (填序号)(1)离子化合物是②③⑥⑦
(2)共价化合物是④⑤
(3)只由极性键构成的物质是④
(4)只由非金属元素组成的离子化合物是⑦
(5)由极性键和非极性键构成的物质是⑤
(6)由离子键和非极性键构成的物质是②
(7)写出下列物质的电子式:NaOH
 . H2O2
. H2O2 NH4Cl
NH4Cl
(8)用电子式表示下列物质的形成过程MgF2
 .
.
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,同种非金属元素之间易形成非极性共价键,不同非金属元素之间易形成极性键;结合物质的成键情况并根据电子式的书写规则书写,离子化合物中阴离子一定要用括号,并标明电荷数,多核阳离子要用括号;用原子的电子式和化合物的电子式来书写形成过程,据此分析解答.
解答 解::①Cl2中由非极性共价键形成的单质;
②Na2O2含有离子键和非极性键的离子化合物;
③NaOH含有离子键和极性键的离子化合物;
④HCl只含有极性键的共价化合物;
⑤H2O2含有极性键和非极性键的共价化合物;
⑥MgF2只含有离子键的离子化合物;
⑦NH4Cl含有离子键和极性键的离子化合物;
⑧Ne没有化学键;综上所述
(1)离子化合物是②③⑥⑦,故答案为:②③⑥⑦;
(2)共价化合物是④⑤,故答案为:④⑤;
(3)只由极性键构成的物质是④,故答案为:④;
(4)只由非金属元素组成的离子化合物是⑦,故答案为:⑦;
(5)由极性键和非极性键构成的物质是⑤,故答案为:⑤;
(6)由离子键和非极性键构成的物质是②,故答案为:②;
(7)氢氧化钠是氢氧根和钠离子间通过离子键形成的化合物,其中的氢氧根中含有共价键,电子式为 ;氯化铵中氯离子和铵根离子之间通过离子键形成化合物,其中铵根中含有共价键,电子式为
;氯化铵中氯离子和铵根离子之间通过离子键形成化合物,其中铵根中含有共价键,电子式为 ;过氧化氢为共价化合物,两个氧原子通过共用电子对形成O-O,两个氧原子分别与两个氢原子通过共用电子对形成H-O键,电子式为
;过氧化氢为共价化合物,两个氧原子通过共用电子对形成O-O,两个氧原子分别与两个氢原子通过共用电子对形成H-O键,电子式为 ,故答案为:
,故答案为: ;
; ;
; ;
;
(8)氟离子和镁离子通过离子键形成离子化合物氟化镁,其形成过程为 ,
,
故答案为; .
.
点评 本题考查了离子键、极性共价键、非极性共价键的判断、电子式的书写知识,根据概念来分析解答即可,难度不大.

练习册系列答案
相关题目
3.下列说法错误的是( )
| A. | O3与SO2的结构相似 | B. | 硫粉不溶于水,易溶于CS2中 | ||
| C. | Be(OH)2是两性氢氧化物 | D. | 在相同条件下,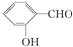 的沸点高于 的沸点高于 |
20.雷雨天闪电时空气中有臭氧生成,下列说法正确的是( )
| A. | 16O2和18O3互为同位素 | |
| B. | O2和O3的相互转化是物理变化 | |
| C. | 等物质的量的O2和O3含有相同的质子数 | |
| D. | 等质量的O2和O3含有相同的O原子数 |
17.化学与数学有密切的联系,将某些化学知识用数轴表示,可以受到直观形象、简明易记的良好效果.下列用数轴表示的化学知识中错误的是( )
| A. | 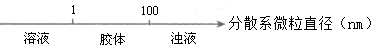 分散系的分类 | |
| B. | 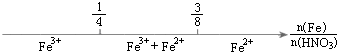 铁与稀硝酸反应后溶液中铁元素的存在形式 | |
| C. | 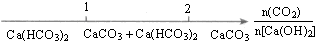 CO2通入澄清石灰水中反应的产物 | |
| D. | 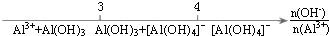 AlCl3溶液中滴加NaOH溶液后Al元素的存在形式 |
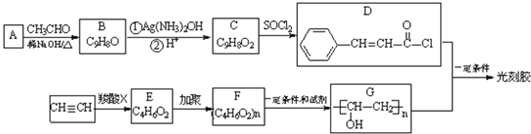
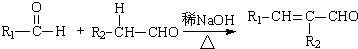 (R,R′为烃基或氢)
(R,R′为烃基或氢) (R,R′为烃基)
(R,R′为烃基)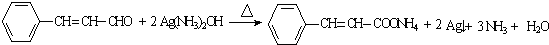 .
. .
. .
.
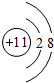 ,A、B、C形成的化合物的电子式为
,A、B、C形成的化合物的电子式为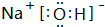 .
.