题目内容
下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.
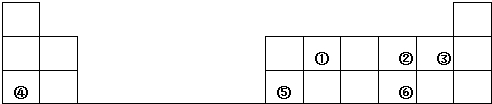
请按要求回答下列问题:
(1)写出②的元素名称 ;②元素形成氢化物的电子式
(2)将①、②和③三种元素相比较,非金属性最强的是 (填元素符号);
(3)元素⑥的氢化物的化学式为 ;
(4)元素④和元素⑤的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是 .

请按要求回答下列问题:
(1)写出②的元素名称
(2)将①、②和③三种元素相比较,非金属性最强的是
(3)元素⑥的氢化物的化学式为
(4)元素④和元素⑤的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是
考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,①②③④⑤⑥分别是C、O、F、Na、Al、S元素,
(1)②是O元素,其氢化物为水或双氧水;
(2)同一周期元素,从左到右非金属性逐渐增强;
(3)⑥为S元素,其最低负价为-2,据此写出氢化物的化学式;
(4)④、⑤两种元素的最高价氧化物对应的水化物分别为氢氧化铝、NaOH,二者反应生成偏铝酸钠与水.
(1)②是O元素,其氢化物为水或双氧水;
(2)同一周期元素,从左到右非金属性逐渐增强;
(3)⑥为S元素,其最低负价为-2,据此写出氢化物的化学式;
(4)④、⑤两种元素的最高价氧化物对应的水化物分别为氢氧化铝、NaOH,二者反应生成偏铝酸钠与水.
解答:
解:根据元素在周期表中的位置知,①②③④⑤⑥分别是C、O、F、Na、Al、S元素,
(1)由上面分析可知②是O元素,其元素的名称为氧元素,其氢化物为水或双氧水,电子式分别为 、
、 ,
,
故答案为:氧; 或
或 ;
;
(2)同一周期元素,从左到右非金属性逐渐增强,所以C、O、F的非金属性依次增强,则F的非金属性最强,故答案为:F;
(3)⑥为S元素,其最低负价为-2,则S的氢化物的化学式为H2S,故答案为:H2S;
(4)④、⑤两种元素的最高价氧化物对应的水化物分别为氢氧化铝、NaOH,二者反应生成偏铝酸钠与水,反应离子方程式为Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O.
(1)由上面分析可知②是O元素,其元素的名称为氧元素,其氢化物为水或双氧水,电子式分别为
 、
、 ,
,故答案为:氧;
 或
或 ;
;(2)同一周期元素,从左到右非金属性逐渐增强,所以C、O、F的非金属性依次增强,则F的非金属性最强,故答案为:F;
(3)⑥为S元素,其最低负价为-2,则S的氢化物的化学式为H2S,故答案为:H2S;
(4)④、⑤两种元素的最高价氧化物对应的水化物分别为氢氧化铝、NaOH,二者反应生成偏铝酸钠与水,反应离子方程式为Al(OH)3+OH-═AlO2-+2H2O,
故答案为:Al(OH)3+OH-═AlO2-+2H2O.
点评:本题考查位置、结构、性质的关系,为高频考点,把握元素的位置推断元素及元素化合物知识为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,则这种碳原子称为“手性碳原子”,凡有一个手性碳原子的物质一定具有光学活性,物质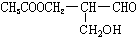 有光学活性,发生下列反应后生成的有机物仍有光学活性的( )
有光学活性,发生下列反应后生成的有机物仍有光学活性的( )
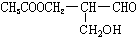 有光学活性,发生下列反应后生成的有机物仍有光学活性的( )
有光学活性,发生下列反应后生成的有机物仍有光学活性的( )| A、与甲酸发生酯化反应 |
| B、与NaOH水溶液共热 |
| C、与足量的氧气作用 |
| D、在催化剂存在下与氢气作用 |
已知:3S+6KOH
2K2S+K2SO3+3H2O,在反应中被还原的硫原子与被氧化的硫原子个数比为( )
| ||
| A、1:1 | B、1:5 |
| C、1:2 | D、2:1 |
常温常压下,0.1mol两种气态烃组成的混合物完全燃烧后得到0.16mol二氧化碳和3.6g水,则混合气体中( )
| A、一定有甲烷 |
| B、一定有丙烯 |
| C、一定有乙炔 |
| D、一定有乙烷 |
在①容量瓶 ②蒸发皿 ③试管 ④量筒 ⑤烧杯五种仪器中,不能加热的是( )
| A、①④ | B、②③⑤ |
| C、③④ | D、①②⑤ |
为了防止FeSO4被氧化而变质,实验室在配制FeSO4溶液时,常在溶液中加入少量的( )
| A、铜粉 |
| B、铁粉 |
| C、锌粉 |
| D、Fe2(SO4) |
已知1mol红磷转化为1mol白磷,吸收18.39kJ热量.①4P(s,红)+5O2(g)═2P2O5(s)△H1 ②4P(s,白)+5O2(g)═2P2O5(s)△H2,则△H1与△H2的关系正确的是( )
| A、△H1=△H2 |
| B、△H1>△H2 |
| C、△H1<△H2 |
| D、无法确定 |
 某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步: