题目内容
11.一定质量的钠、钾投入一定量的稀盐酸中,产生气体随时间变化的曲线如图,则下列说法中正确的是( )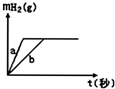
| A. | 曲线a为K,b为Na | B. | 投入的Na的质量大于K的质量 | ||
| C. | 投入的Na、K一定等质量 | D. | 稀盐酸的量一定是不足量的 |
分析 A.金属钾的活泼性大于钠,与水反应速率快与钠;
B.依据产生氢气的量相同计算金属的质量;
C.生成1mol氢气,消耗钠的质量为46g,消耗钾的质量为78g;
D.钠、钾不仅和盐酸反应还和水反应,产生氢气的量取决于钠、钾的用量.
解答 解:A.钾的金属性大于钠,则钾与酸反应速率大于钠与酸反应速率,即生成相同物质的量的氢气,钾需要的时间短,钠需要的时间长,所以曲线a为钾,b为钠,故A正确;
B.有图象可知两种金属与盐酸反应生成氢气的量相等,则:
2Na+2HCl=2NaCl+H2↑,
46g 1mol
2K+2HCl=2KCl+H2↑,
78g 1mol,
所以生成相同量的氢气,消耗钾的质量多,故B错误;
C.通过方程式知,生成相同物质的量的氢气需要金属的质量不同,故C错误;
D.因为钠、钾不仅和盐酸反应还和水反应,所以钠、钾生成相同物质的量的氢气与稀盐酸是否足量无关,故D错误;
故选A.
点评 本题考查了碱金属元素的性质,明确钠、钾性质,曲线图的含义是解题关键,题目难度不大.

练习册系列答案
相关题目
19.某研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体甲并夹杂有少量黑色物质乙.倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,仍有未溶解的黑色固体丙.过滤、洗涤后,向黑色固体丙中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成.下列所得结论不正确的是( )
| A. | 铜与浓硫酸反应所得白色固体甲是CuSO4 | |
| B. | 加BaCl2溶液后所得白色沉淀是BaSO3 | |
| C. | 白色固体甲中夹杂的少量黑色物质乙中不可能含有CuO | |
| D. | 白色固体甲中夹杂的少量黑色物质乙中含元素Cu、S |
6. (1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(2)Mg2Cu是一种储氢合金.350℃时,Mg2Cu与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为0.077).Mg2Cu与H2反应的化学方程式为2Mg2Cu+3H2$\frac{\underline{\;\;△\;\;}}{\;}$MgCu2+3MgH2.
(3)锡常见的价态有+2和+4价,在化合物中稳定的价态为+4价,则配制的SnCl2的水溶液除了固体SnCl2和水外,还需要的物质是盐酸和Sn.
(4)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为其△H-T△S>0.
(5)Mg(OH)2是制镁盐、耐火材料和阻燃剂的重要原料.
已知:a、25℃时,KSP[Mg(OH)2]=4.0×10-38;b、Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81.5kJ•mol-1.
①下列叙述正确的是BD.
A、从盐卤或海水中获得Mg(OH)2,工业上选择NaOH作沉淀剂
B.Mg(OH)2能作阻燃剂是它分解吸热且生成MgO覆盖可燃物
C、可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁
D、高温下,碳可以和氧化镁发生反应
②酸碱指示剂百里酚蓝变色的pH范围如下:
25℃时,在Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为蓝色.
 (1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”). | T/K | T1 | 573 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
(3)锡常见的价态有+2和+4价,在化合物中稳定的价态为+4价,则配制的SnCl2的水溶液除了固体SnCl2和水外,还需要的物质是盐酸和Sn.
(4)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g),已知该反应的△H>0,简述该设想能否实现的依据:不能实现,因为其△H-T△S>0.
(5)Mg(OH)2是制镁盐、耐火材料和阻燃剂的重要原料.
已知:a、25℃时,KSP[Mg(OH)2]=4.0×10-38;b、Mg(OH)2(s)=MgO(s)+H2O(g)△H=+81.5kJ•mol-1.
①下列叙述正确的是BD.
A、从盐卤或海水中获得Mg(OH)2,工业上选择NaOH作沉淀剂
B.Mg(OH)2能作阻燃剂是它分解吸热且生成MgO覆盖可燃物
C、可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁
D、高温下,碳可以和氧化镁发生反应
②酸碱指示剂百里酚蓝变色的pH范围如下:
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
16.下列关于各图象的解释或得出结论正确的是( )

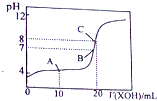
| A. | 图1表示0.10mol•L-1NaOH溶液滴定20.00mL0.10mol•L-1醋酸溶液的滴定曲线 | |
| B. | 图2表示乙酸溶液中通入氨气至过量过程中溶液导电性I的变化 | |
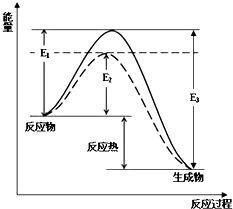
| C. | 根据图3所示可知:石墨比金刚石稳定 | |
| D. | 图4表示反应:2SO2+O2?2SO3,t1时刻只减小的SO3的浓度 |
3.下列说法正确的是( )
| A. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积,其比值一定为2:1 | |
| B. | 将NaOH溶液和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的二分之一 | |
| C. | 如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍 | |
| D. | 制取TiO2可用TiCl4加大量水,同时加热:TiCl4+(x+2)H2O(过量)?TiO2•xH2O↓+4HCl,所得的TiO2•H2O经焙烧得TiO2 |
20.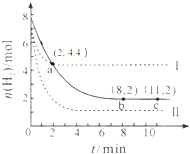 某温度下,将6mol CO2和8mol H2 充入2L密闭容器中发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,容器中H2的物质的量随时间的变化关系如右图中的实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系.下列说法正确的是( )
某温度下,将6mol CO2和8mol H2 充入2L密闭容器中发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,容器中H2的物质的量随时间的变化关系如右图中的实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系.下列说法正确的是( )
 某温度下,将6mol CO2和8mol H2 充入2L密闭容器中发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,容器中H2的物质的量随时间的变化关系如右图中的实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系.下列说法正确的是( )
某温度下,将6mol CO2和8mol H2 充入2L密闭容器中发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,容器中H2的物质的量随时间的变化关系如右图中的实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化关系.下列说法正确的是( )| A. | 曲线Ⅰ对应的条件改变可能降低温度 | |
| B. | 曲线Ⅱ对应的条件改变可能是充入氦气 | |
| C. | 该温度下,此反应的化学平衡常数的数值为0.5 | |
| D. | 从反应开始至a 点,ν(CO2)=0.6 mol•L-1•min-1 |
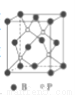
 X、Y是元素周期表前20号元素,且X的原子序数比Y大4,请填空(X、Y要用具体的元素符号表示):
X、Y是元素周期表前20号元素,且X的原子序数比Y大4,请填空(X、Y要用具体的元素符号表示):