题目内容
7.氯化亚铜在工业上应用广泛.利用反应Cu2++Cu+2Cl-=2CuCl制氯化亚铜的流程如图1.氯化亚铜(CuC1)为白色晶体,不溶于硫酸、稀硝酸和醇,微溶于水,在空气中会被迅速氧化,能溶于浓盐酸,并生成配合物,该配合物加水稀释后会重新析出CuCl沉淀.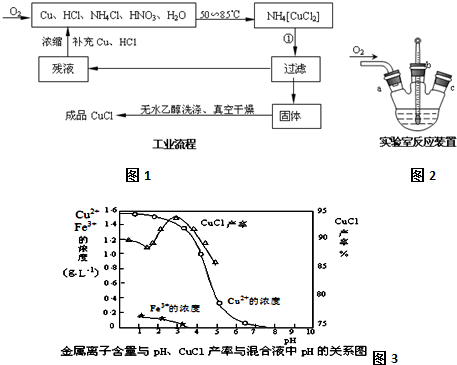
实验药品:铜丝20g、氯化铵20g、65% 硝酸10mL、36%盐酸15mL、水.
(1)反应①的化学方程式为NH4[CuCl2]=CuCl↓+NH4Cl.
(2)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装的
目的是加快乙醇和水的蒸发,防止CuCl被空气氧化.
(3)工业化生产时,乙醇可通过蒸馏方法回收并循环利用,而NH4Cl、HNO3(填化学式)可直接循环利用.
(4)实验室用图2装置制备CuCl.实验开始时,温度计显示反应液温度低于室温,主要原因是氯化铵溶于水吸收大量热量,造成反应液温度降低,电炉加热升温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色,从环保角度考虑,当烧瓶上方红棕色气体逐渐变为无色时才能停止通入氧气.
(5)氯化亚铜在工业上也可以利用酸性电镀废液(主要含Cu2+、Fe3+)制得高浓度硫酸铜溶液后,加入铁粉、氯化钠生成CuCl.反应的离子反应方程式为:2Cu2++2Cl-+Fe=2CuCl↓+Fe2+.CuCl产率与混合液pH的关系如图3,析出CuCl晶体时的最佳pH在3左右.
分析 (1)依据流程分析NH4[CuCl2]分解产物过滤后得到滤液为氯化铵,固体为CuCl;
(2)由题给信息可知CuCl微溶于水,不溶于乙醇,在空气中会被迅速氧化;
(3)依据乙醇沸点低利用蒸馏方法回收利用,制备过程中的氯化铵和硝酸直接利用;
(4)制备氯化亚铜所用的原料中含有氯化铵溶解过程中吸热,生成的红棕色气体二氧化氮污染气体不能排放,需要通入氧气至恰好吸收生成硝酸循环使用;
(5)在硫酸铜溶液中加入氯化钠、铁,发生氧化还原反应生成CuCl;由图可知,析出CuCl沉淀的最佳pH应为CuCl的产率最大,且氢氧化铁杂质较少.
解答 解:(1)NH4[CuCl2]分解产物过滤后得到滤液为氯化铵,固体为CuCl,反应的化学方程式为NH4[CuCl2]=CuCl↓+NH4Cl,
故答案为:NH4[CuCl2]=CuCl↓+NH4Cl;
(2)由题给信息可知CuCl微溶于水,不溶于乙醇,在空气中会被迅速氧化,为防止氧化应隔绝空气,在干燥、真空环境中可加快乙醇和水的蒸发,
故答案为:加快乙醇和水的蒸发,防止CuCl被空气氧化;
(3)根据乙醇的沸点较低,可以利用蒸馏的方法回收乙醇循环利用,反应过程中的氯化铵和硝酸可以在混合液中 直接利用,
故答案为:蒸馏;HNO3;
(4)制备氯化亚铜所用的原料为Cu、HCl、NH4Cl、HNO3、H2O,其中含有氯化铵溶解过程中吸热,反应过程中生成的红棕色气体二氧化氮污染气体不能排放,需要通入氧气至恰好吸收生成硝酸循环使用,4NO2+O2+2H2O=4HNO3,
故答案为:氯化铵溶于水吸收大量热量,造成反应液温度降低;烧瓶上方红棕色气体逐渐变为无色;
(5)在硫酸铜溶液中加入氯化钠、铁,发生氧化还原反应生成CuCl,发生2Cu2++2Cl-+Fe=2CuCl↓+Fe2+;由图可知,析出CuCl沉淀的最佳pH应为CuCl的产率最大,且氢氧化铁杂质较少,应约为3左右,故答案为:2Cu2++2Cl-+Fe=2CuCl↓+Fe2+;3.
点评 本题考查了物质制备的流程分析和反应产物判断,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握反应条件、反映实际的选择,反应过程中物质循环利用的绿色化学思想,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | Mg2+、K+、Cl-、AlO2- | B. | Al3+、Na+、NO3-、HCO3- | ||
| C. | NH4+、Fe3+、SO42-、NO3- | D. | Ca2+、H+、NO3-、S2O32- |
| A. | 1个氖原子 Na | B. | +2价的铁元素 Fe+2 | ||
| C. | 4个氢分子 4H | D. | 3个硝酸根离子 3NO3- |
| A. | 提高CO2充气压力,饮料中c(A-)不变 | |
| B. | 当pH为5.0时,饮料中 $\frac{c(HA)}{c({A}^{-})}$=0.16 | |
| C. | 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低 | |
| D. | 结合H+的能力:A->HCO3- |