题目内容
5.根据如表实验操作和现象得出的结论正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该食盐中一定没有添加KIO3 |
| D | 向Na2SiO3溶液中滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性一定比硅酸强 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.生成的气体可能为二氧化碳或二氧化硫,原溶液中可能含有亚硫酸根离子、碳酸氢离子;
B.铁与浓硫酸在常温下发生钝化现象;
C.碘单质遇淀粉显示蓝色,碘酸钾遇到淀粉不显示蓝色;
D.溶液变浑浊,说明生成硅酸,则碳酸的酸性大于硅酸.
解答 解:A.将某溶液与稀盐酸反应产生的气体通入澄清石灰水,石灰水变浑浊,生成的气体可能为二氧化碳或二氧化硫,原溶液中可能含有亚硫酸根离子、碳酸氢根离子,不一定含有碳酸根离子,故A错误;
B.常温下,将铁片浸入足量浓硫酸中,铁与浓硫酸发生反应生成一层致密的氧化膜,阻止了反应的继续进行,故B错误;
C.向某食盐溶液中滴加淀粉溶液,溶液颜色不变,说明食盐中不存在碘单质,不能说明该食盐中没有添加KIO3,故C错误;
D.向Na2SiO3溶液中滴加乙酸溶液,溶液变浑浊,说明反应生成硅酸沉淀,则酸性:碳酸>硅酸,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及离子检验、铁的钝化、碘单质与淀粉的特征反应、酸性强弱比较等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
15.铜锈是一种绿色化合物,它的成分为碱式碳酸铜,兼有氢氧化铜和碳酸铜的性质.试推测:铜锈在高温灼烧条件下充分反应后的固体物质是( )
| A. | 黑色的氧化铜 | B. | 红色的氧化亚铜 | ||
| C. | 蓝色的氢氧化铜和碳酸铜 | D. | 黑色的氧化亚铜 |
16.为鉴别乙醇、乙酸、葡萄糖溶液,选用一种试剂,可为下列中的( )
| A. | 氢氧化钠 | B. | 硝酸 | C. | 碘 | D. | 新制氢氧化铜 |
10. 某些牙膏中含有茶多酚,茶多酚是茶叶中多酚类物质的总称,是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(GC)的结构简式如图所示,下列关于GC的叙述中正确的是( )
某些牙膏中含有茶多酚,茶多酚是茶叶中多酚类物质的总称,是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(GC)的结构简式如图所示,下列关于GC的叙述中正确的是( )
 某些牙膏中含有茶多酚,茶多酚是茶叶中多酚类物质的总称,是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(GC)的结构简式如图所示,下列关于GC的叙述中正确的是( )
某些牙膏中含有茶多酚,茶多酚是茶叶中多酚类物质的总称,是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(GC)的结构简式如图所示,下列关于GC的叙述中正确的是( )| A. | 分子中所有的原子共面 | |
| B. | 1 mol GC与6 mol NaOH恰好完全反应 | |
| C. | 能发生氧化反应、取代反应、消去反应,难发生加成反应 | |
| D. | 遇FeCl3溶液不发生显色反应 |
17.16O和18O是氧元素的两种核素,NA表示阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 16O和18O的质量数相同,但是中子数不同 | |
| B. | 16O和18O核外电子排布不同 | |
| C. | 通过化学变化可以实现16O与18O间的相互转化 | |
| D. | 标准状况下,1.12L16O2和1.12L18O2均含0.1NA个氧原子 |
14.下列可逆反应平衡常数,其表达式或与有关常数的关系正确的是( )
| A. | 反应C(s)+H2O(g)?CO(g)+H2(g) 的平衡常数为:K=$\frac{c(CO)•c({H}_{2})}{c(C)•c({H}_{2}O)}$ | |
| B. | 反应Cr2O72-+H2O?2CrO42-+2H+ 的平衡常数为:K=$\frac{c(Cr{O}_{4}^{2-})•{c}^{2}({H}^{+})}{c(C{r}_{2}{O}_{3}^{2-})•c({H}_{2}O)}$ | |
| C. | NH4++H2O?NH3•H2O+H+的平衡常数为:K=$\frac{{K}_{W}}{{K}_{b}(N{H}_{3}•{H}_{2}O)}$ | |
| D. | 2AgI(s)+S2-(aq)?Ag2S(s)+2I-(aq)的平衡常数为:K=$\frac{{K}_{sp}(A{g}_{2}S)}{{{K}_{sp}}^{2}(AgI)}$ |
15.“2016年地球一小时”推出“为”蓝生活主题,鼓励公众践行可持续的生活和消费方式.下列做法与之不符的是( )
| A. | 利用太阳能制氢 | B. | 用家用汽车代替公交车 | ||
| C. | 利用化石燃料制造燃料电池 | D. | 用节能灯代替白炽灯 |

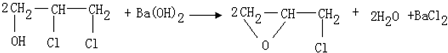 ;
;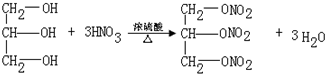 .
.