题目内容
A、B、C、D 四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和.
(1)A为 元素,B为 元素,C为 元素.D的质子数和中子数相等,D的原子组成符号为 ,它的最高正价为 价.
(2)用电子式表示A、B两元素形成AB2的过程: 用电子式表示C、D两元素形成化学键的过程: .
(3)写出E和A的最高价氧化物反应的化学方程式,并标出电子转移的方向和数目: .
(1)A为
(2)用电子式表示A、B两元素形成AB2的过程:
(3)写出E和A的最高价氧化物反应的化学方程式,并标出电子转移的方向和数目:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为四种短周期元素,原子序数依次增大,B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,则固体E为Na2O2,则B为O元素、C为Na元素;A的原子序数小于B,且A原子的最外层上有4个电子,则A为C元素;D的L层电子数等于K、M两个电子层上电子数之和,则D原子M层电子数为8-2=6,核外各层电子分别为2、8、6,则D为S元素,据此解答各小题即可.
解答:
解:依据分析可知:A为碳,B为氧,C为钠,D为硫,
(1)由上述分析可知,A为C元素、B为O元素、C为Na元素,D的质子数和中子数相等,质子数为16,中子数为16,故质量数为32,S的原子组成符号为:
S,由于价电子数为6,故最高正价为+6价,故答案为:碳;氧;钠;
S;+6;
(2)A为C,B为O,A、B两元素形成的AB2为二氧化碳,二氧化碳属于共价化合物,用电子式表示二氧化碳的形成过程为: ,C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为:
,C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为: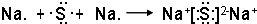 ,
,
故答案为: ;
;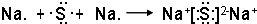 ;
;
(3)Na2O2与CO2反应生成了碳酸钠和氧气,在Na2O2与CO2的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为: ,故答案为:
,故答案为: .
.
(1)由上述分析可知,A为C元素、B为O元素、C为Na元素,D的质子数和中子数相等,质子数为16,中子数为16,故质量数为32,S的原子组成符号为:
32 16 |
32 16 |
(2)A为C,B为O,A、B两元素形成的AB2为二氧化碳,二氧化碳属于共价化合物,用电子式表示二氧化碳的形成过程为:
 ,C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为:
,C为Na,D为S,Na与S形成的化合物为Na2S,属于离子化合物,用Na原子、S原子电子式表示硫化钠的形成过程为: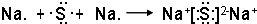 ,
,故答案为:
 ;
;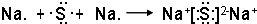 ;
;(3)Na2O2与CO2反应生成了碳酸钠和氧气,在Na2O2与CO2的反应中,化合价升高数=化合价降低数=转移电子数=2,电子转移情况为:
 ,故答案为:
,故答案为: .
.
点评:本题考查结构性质位置关系应用,题目难度中等,根据题干信息正确判断各元素名称为解答关键,试题侧重对常见化学用语的考查,注意对基础知识的积累掌握.

练习册系列答案
相关题目
用标准溶液NaOH滴定未知浓度的盐酸,以下操作会造成测定结果偏低的是( )
| A、配制标准溶液时,固NaOH体中混有NaCl 杂质 |
| B、滴定终点读数时,俯视滴定管的刻度 |
| C、盛放未知液的锥形瓶用蒸馏水洗过,未用未知液体润洗 |
| D、配制NaOH标准溶液时,定容时俯视刻度线 |
对于可逆反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列正确的是( )
A、平衡常数的表达式K=
| ||
| B、当v正(NH3):v正(NO)=1:1时,说明该反应已经达到平衡 | ||
| C、若平衡时两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=5:4 | ||
| D、反应达到平衡后,恒容条件下,同倍数改变NH3和NO的量,c(O2)=可能不变 |
 某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.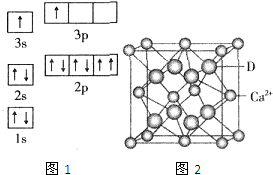 已知A、B、C、D、E五种元素的性质或结构信息如下,请根据信息回答下列问题:
已知A、B、C、D、E五种元素的性质或结构信息如下,请根据信息回答下列问题: