题目内容
若NA表示阿佛加德罗常数,下列说法正确的是( )
| A、1 mol氦气分子中含2NA个氦原子 |
| B、25℃时,l L pH=13的Ba(OH)2 溶液中含有OH-的数目为0.1NA |
| C、1.8 g重水(21H2O)中所含质子的个数为NA |
| D、1L 0.2mol/L的FeCl3溶液中Fe3+的数目为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.稀有气体为单原子分子,1mol氦气中含有1mol氦原子;
B.25℃时pH=13的溶液中氢氧根离子浓度为0.1mol/L,则1L该溶液中含有0.1mol氢氧根离子;
C.重水的摩尔质量为20g/mol,重水分子中含有10个质子,1.8g重水的物质的量为0.09mol,含有0.9mol质子;
D.氯化铁溶液中铁离子部分水解,导致铁离子数目减少.
B.25℃时pH=13的溶液中氢氧根离子浓度为0.1mol/L,则1L该溶液中含有0.1mol氢氧根离子;
C.重水的摩尔质量为20g/mol,重水分子中含有10个质子,1.8g重水的物质的量为0.09mol,含有0.9mol质子;
D.氯化铁溶液中铁离子部分水解,导致铁离子数目减少.
解答:
解:A.氦气为单原子分子,1mol氦气中含有1mol氦原子,含NA个氦原子,故A错误;
B.25℃时,pH=13的氢氧化钡溶液中的氢氧根离子浓度为0.1mol/L,则1L该溶液中含有0.1mol氢氧根离子,含有OH-的数目为0.1NA,故B正确;
C.1.8g重水的物质的量为:
=0.09mol,0.09mol重水分子中含有0.9mol质子,所含质子的个数为0.9NA,故C错误;
D.1L 0.2mol/L的FeCl3溶液中含有溶质氯化铁0.2mol,由于铁离子部分水解,溶液中铁离子小于0.2mol,Fe3+的数目小于0.2NA,故D错误;
故选B.
B.25℃时,pH=13的氢氧化钡溶液中的氢氧根离子浓度为0.1mol/L,则1L该溶液中含有0.1mol氢氧根离子,含有OH-的数目为0.1NA,故B正确;
C.1.8g重水的物质的量为:
| 1.8g |
| 20g/mol |
D.1L 0.2mol/L的FeCl3溶液中含有溶质氯化铁0.2mol,由于铁离子部分水解,溶液中铁离子小于0.2mol,Fe3+的数目小于0.2NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,选项A为易错点,需要明确稀有气体为单原子分子.

练习册系列答案
相关题目
下列说法正确的是( )
| A、所有元素中原子半径最小的是F |
B、根据π键的成键特征判断C-C的键能与  键能的关系是双键的键能小于单键的键能的2倍 键能的关系是双键的键能小于单键的键能的2倍 |
| C、元素电负性越小,元素非金属性越强 |
| D、第n周期第n主族的元素均为金属 |
一个原电池的总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的合理组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Zn | Cu | CuCl2 |
| B | Cu | Zn | H2SO4 |
| C | Cu | Zn | CuSO4 |
| D | Zn | Fe | CuCl2 |
| A、A | B、B | C、C | D、D |
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
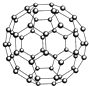

| A、28 g N60单质(见如图)中含有的N-N键键数为3NA |
| B、常温常压下,28 g C2H4和C3H6的混合气体中含有碳原子的数目为2NA |
| C、一定温度下,1 L0.5mol/L 的NH4Cl溶液与2 L 0.25 moL/L NH4Cl溶液含NH4+数目相等 |
| D、含有2NA个阴离子的CaC2在标准状况下,能产生约44.8L的乙炔气体 |
下列各组物质的燃烧热相等的是( )
| A、红磷 和 白磷 |
| B、1g H2和2g H2 |
| C、3molC2H2和1molC6H6 |
| D、葡萄糖和果糖 |
2014年第45个世界地球日的主题是“珍惜地球资源,转变发展方式--节约集约利用国土资源共同保护自然生态空间”.你认为下列行为中不符合这一主题的是( )
| A、控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 |
| B、研究采煤、采油新技术,大量开发新矿山,提高产量以满足工业生产的快速发展 |
| C、开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料 |
| D、实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle),以此来推进生态文明建设 |
 A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.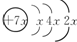 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个单电子,E的外围电子排布式为3d64s2.回答下列问题: