题目内容
13.在密闭容器中发生反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )| A. | a<c+d | B. | A的转化率增大 | ||
| C. | D的体积分数变大 | D. | 平衡向正反应方向移动 |
分析 假定平衡不移动,将气体体积压缩到原来的一半,D的浓度为原来的2倍,实际再次达到新平衡时,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,即a<c+d,压强增大,速率加快,新平衡的正、逆速率都大于原平衡,据此结合选项解答.
解答 解:假定平衡不移动,将气体体积压缩到原来的一半,D的浓度为原来的2倍,实际再次达到新平衡时,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,即a<c+d,压强增大,速率加快,新平衡的正、逆速率都大于原平衡,
A、D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,即a<c+d,故A正确;
B、平衡向逆反应移动,A的转化率降低,故B错误;
C、气体体积压缩到原来的一半,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,则D的体积分数变小,故C错误;
D、气体体积压缩到原来的一半,D的浓度为原来的1.8倍,说明压强增大,平衡向逆反应移动,故D错误;
故选A.
点评 本题考查化学平衡的影响因素,难度不大,根据D的浓度变化判断平衡移动方向是解题的关键,注意根据平衡移动图象理解速率的变化.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
1.下列说法正确的是( )
| A. | 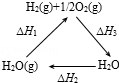 图中△H1=△H2+△H3 | |
| B. |  如图在催化剂条件下,反应的活化能等于E1+E2 | |
| C. | 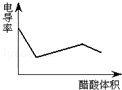 如图表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 | |
| D. |  如图可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量 |
8.根据我国统一实行法定计量单位的规定,下列说法比较规范的是( )
| A. | 98g硫酸的摩尔数为1 mol | B. | 氧的摩尔质量为32g/mol | ||
| C. | 阿伏加德罗常数约为6.02×1023个 | D. | 某硫酸中H2SO4的质量分数为0.60 |
5.CO2与NO混合气体VL,通过足量Na2O2充分反应后,剩余气体体积可能为(假设NO与Na2O2不发生反应,不考虑NO2与N2O4相互转化)( )
| A. | $\frac{V}{2}$L | B. | $\frac{V}{3}$L | C. | $\frac{5V}{6}$L | D. | VL |
2.常温下,Ksp(CaSO4)=9×10-6,CaSO4在水中的沉淀溶解平衡曲线如图所示.下列判断错误的是( )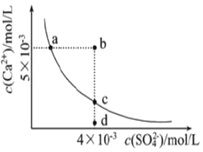

| A. | a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液 | |
| B. | a点对应的Ksp不等于c点对应的Ksp | |
| C. | b点将有沉淀生成,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6 | |
| D. | 向d点溶液中加入适量CaCl2固体可以变成c点 |
3. 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )| A. | A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{{H}_{4}}^{+})}$减小 | |
| B. | 原氨水的物质的量浓度约为1.006×10-2mol•L-1 | |
| C. | A、B、C三点溶液中水电离出来的c(OH-):A>B>C | |
| D. | C点时,盐酸和氨水恰好完全反应 |
 O4)3
O4)3