题目内容
3. 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mL a mol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )| A. | A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{{H}_{4}}^{+})}$减小 | |
| B. | 原氨水的物质的量浓度约为1.006×10-2mol•L-1 | |
| C. | A、B、C三点溶液中水电离出来的c(OH-):A>B>C | |
| D. | C点时,盐酸和氨水恰好完全反应 |
分析 A、加少量水促进氨水的电离,但溶液中铵根离子和氢氧根离子的浓度都减小,温度不变水的离子积是一个常数,所以隐性离子氢离子的浓度变大;
B、由图可知,盐酸和氨水等体积混合,溶液的PH=7,则c(OH-)=c(H+)=1×10-7mol/L,所以c(NH4+)=c(Cl-)=$\frac{0.01}{2}$=0.005mol/L,则c(NH3•H2O)=$(\frac{a}{2}-0.005)mol/L$,根据Kb的表达式代入相关数据进行计算;
C、显性离子氢氧根离子浓度越大,水电离出的氢离子的浓度越小;
D、由图可知C点时,溶液呈中性.
解答 解:A、加少量水促进氨水的电离,但溶液中铵根离子和氢氧根离子的浓度都减小,温度不变水的离子积是一个常数,所以隐性离子氢离子的浓度变大,所以A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{{H}_{4}}^{+})}$增大,故A错误;
B、由图可知,盐酸和氨水等体积混合,溶液的PH=7,则c(OH-)=c(H+)=1×10-7mol/L,所以c(NH4+)=c(Cl-)=$\frac{0.01}{2}$=0.005mol/L,则c(NH3•H2O)=$(\frac{a}{2}-0.005)mol/L$,根据Kb=$\frac{0.005×1×1{0}^{-7}}{\frac{a}{2}-0.005}$=1.75×10-5,解得a=1.006×10-2mol•L-1,故B正确;
C、显性离子氢氧根离子浓度越大,水电离出的氢离子的浓度越小,所以水电离出的氢氧根离子浓度的大小为:A<B<C,故C错误;
D、C点时,如果盐酸和氨水恰好完全反应生成氯化铵,溶液呈酸性,而C点溶液呈中性,所以氨水过量,故D错误;
故选B.
点评 本题考查较综合,涉及弱电解质的电离、酸碱混合溶液定性判断、离子浓度的大小的比较等知识点,侧重考查学生分析计算能力,注意弱电解质电离平衡常数与其对应弱离子水解程度关系,题目难度中等.

| A. | a<c+d | B. | A的转化率增大 | ||
| C. | D的体积分数变大 | D. | 平衡向正反应方向移动 |
| A. | 溶液和胶体的本质区别为是否能产生丁达尔效应 | |
| B. | K2Cr2O7溶液和氢溴酸能存放于同一药品橱内 | |
| C. | 用带玻璃塞的细口试剂瓶保存氢氟酸 | |
| D. | CH4和C2H4均属于常用危险品中的易燃气体 |
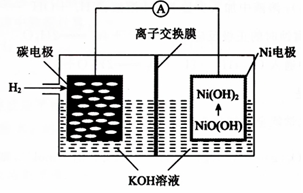
| A. | 离子交换膜选用阳离子交换膜(只允许阳离子通过) | |
| B. | 正极的电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| C. | 导线中通过1mol电子时,理论上负极区溶液质量增加1g | |
| D. | 充电时,碳电极与电源的正极相连 |
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.
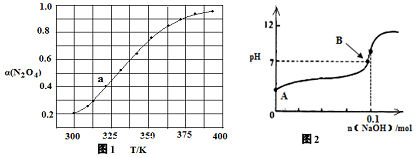
如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
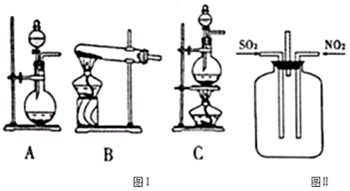
(1)SO2的发生装置可以选择图Ⅰ中的A(或C )(填字母),反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O[或Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O].
(2)按图Ⅱ所示进行实验.
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为SO2+NO2=SO3+NO.如果集气瓶中有少量水,则可能观察不到白烟,其原因是生成的SO3与水反应生成硫酸.
②请指出图Ⅱ装置设计的不合理之处没有进行尾气处理,会导致环境污染.
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:
| 操作步骤 | 实验现象 | 结论 |
| 取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份. | ||
| 一份加入足量稀盐酸后,再加入BaCl2溶液. | 有白色沉淀生成. | 证明雾霾固体中含有SO42- |
| 另一份加入适量的NaOH浓溶液并加热. | 产生使湿润的红色石蕊试纸变蓝色的气体. | 证明雾霾固体中含有NH4+.综合上面实验,说明雾霾固体颗粒中含有(NH4)2SO4. |