题目内容
8.根据我国统一实行法定计量单位的规定,下列说法比较规范的是( )| A. | 98g硫酸的摩尔数为1 mol | B. | 氧的摩尔质量为32g/mol | ||
| C. | 阿伏加德罗常数约为6.02×1023个 | D. | 某硫酸中H2SO4的质量分数为0.60 |
分析 A.98g硫酸的物质的量为1mol,摩尔数没有单位,应该为1;
B.没有指明是氧原子还是氧气分子;
C.阿伏伽德罗常数的单位错误,应该约为6.02×1023/mol;
D.质量分数可以表示为小数,如硫酸溶液中溶质的质量分数为0.60.
解答 解:A.摩尔数只是数值,没有单位,98g硫酸的摩尔数为1,故A错误;
B.必须指明粒子的具体名称,如氧气的摩尔质量为32g/mol,故B错误;
C.阿伏伽德罗常数为约为6.02×1023/mol,故C错误;
D.质量分数可以为百分数,也可以为分数,故D正确;
故选D.
点评 本题考查了物质的量与摩尔、摩尔质量的关系,质量分数、阿伏伽德罗常数的判断,题目难度不大,注意掌握摩尔质量、阿伏伽德罗常数、物质的量的概念及表示方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下面一些报道中,你认为科学的是( )
A.疏通煤气管道时,充入氩气引起爆炸
B.新粉刷过石灰浆的墙壁释放出CO2使一老汉窒息而死
C.有易燃易爆物的工作场所,严禁穿化纤衣服
D.本饮料纯天然,绝对不含化学物质
3.选修四化学反应原理主要研究:化学反应进行的方向、快慢、程度以及反应过程中能量转化等内容.下列有关说法错误的是( )
| A. | 化学变化中,遵循能量守恒,所谓吸热反应可看作把环境中的能量储存到了物质中 | |
| B. | 化学变化中,各种原子的数目是恒定的,所谓资源匮乏只是元素的分布发生了变化 | |
| C. | 氧化还原反应都是放热反应 | |
| D. | 强酸和强碱的中和反应的活化能接近于零,所以反应速率很高 |
13.在密闭容器中发生反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
| A. | a<c+d | B. | A的转化率增大 | ||
| C. | D的体积分数变大 | D. | 平衡向正反应方向移动 |
20.将5.4gAg投入一定量的浓硝酸中完全溶解得到NO和NO2的混合气体,用NaOH溶液把该混合气体完全吸收得到NaNO3和NaNO2的混合溶液,则所得NaNO2的物质的量为( )
| A. | 0.024mol | B. | 0.006mol | C. | 0.075mol | D. | 0.3mol |
18.一种碳纳米管新型二次电池的装置如图所示,下列说法中正确的是( )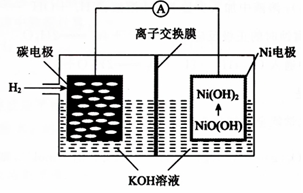

| A. | 离子交换膜选用阳离子交换膜(只允许阳离子通过) | |
| B. | 正极的电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| C. | 导线中通过1mol电子时,理论上负极区溶液质量增加1g | |
| D. | 充电时,碳电极与电源的正极相连 |

 ;氯离子的电子式
;氯离子的电子式 .
.