题目内容
15.下列说法正确的是( )| A. | 烧瓶、锥形瓶、蒸发皿加热时均需要垫上石棉网 | |
| B. | 分液漏斗、滴定管、容量瓶使用前均需要检查是否漏水 | |
| C. | 配制1 mol•L-1NaCl溶液、测定Na2CO3溶液的pH、焰色反应实验均需要用到玻璃棒 | |
| D. | 乙酸乙酯、硝基苯的制备、银镜反应实验均需要水浴加热 |
分析 A.蒸发皿可以直接加热;
B.带有旋塞和瓶塞的仪器,一般在使用前需要检查是否漏水;
C.颜色反应不需要玻璃棒;
D.制备乙酸乙酯可用试管直接加热.
解答 解:A.烧瓶、锥形瓶需要垫上石棉网加热,蒸发皿可以直接加热,故A错误;
B.分液漏斗、滴定管、容量瓶是带有旋塞和瓶塞的仪器,使用前需要检查是否漏水,故B正确;
C.焰色反应不需要玻璃棒,应用铁丝或铂丝,故C错误;
D.制备乙酸乙酯可用试管直接加热,硝基苯的制备温度为40~50℃,需要用水浴加热,银镜反应中,反应温度不宜过高,需要在控制反应温度,所以需要水浴加热,故D错误.
故选B.
点评 本题考查化学实验的基本操作,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
5.中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据判断PM2.5的酸碱性,试样的pH=4.
将PM2.5样本用蒸馏水处理制成待测试样.测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L-1 | 4×10-5 | 6×10-5 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
6.下列反应的离子方程式书写不正确的是( )
| A. | 氯气通入澄清石灰水中:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 小苏打溶液中加入少量石灰水:HCO$\overline{3}$+Ca2++OH-═CaCO3↓+H2O | |
| D. | 用SO2还原含Cr2O72-的酸性废水:Cr2O72-+3SO2+2H+═2Cr3++3SO42-+H2O |
10.以天然气代替汽油作为汽车燃料将有效缓解对石油资源的压力.天然气主要成分是( )
| A. | H2 | B. | O2 | C. | CO | D. | CH4 |
7.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3 的是( )
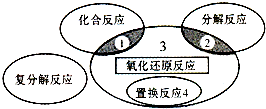

| A. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O | D. | Fe+CuSO4═Cu+FeSO4 |
4.下列有关实验操作说法中,不正确的是( )
| A. | 向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体 | |
| B. | 用量筒、试管、胶头滴管、玻璃棒、蒸馏水和 pH试纸,可鉴别pH 相等的硫酸和醋酸 | |
| C. | 用FeSO4、NaOH和盐酸等试剂在空气中可以制备纯净的FeCl3溶液 | |
| D. | 用NaOH溶液和盐酸可除去MgCl2溶液中混有的AlCl3 |
5.已知某无色溶液中含有Na+,还可能大量存在Ag+、H+、CO32-、Cl-.取出少量原溶液并滴入盐酸会产生气体,但是不会产生白色沉淀.则溶液中( )
| A. | 一定不存在Ag+和NO3- | B. | 一定存在CO32- | ||
| C. | 一定存在NO3-和Cl- | D. | 一定不存在NO3-、H+ |