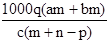题目内容
某化学兴趣小组拟用下图装置测定某粗锌样品中锌的质量分数。他们查阅资料后获知该粗锌样品中的其他成分不能与稀盐酸反应。请填写以下实验报告。
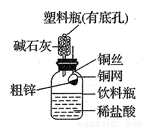
(1)实验目的: 。
(2)实验步骤:
①称取10.0g粗锌置于铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g。
②将铜网插入足量的稀盐酸中,有关反应的化学方程式为 。
③反应完全后,称得装置总质量为119.8g,则粗锌中锌的质量分数为 。
(3)问题探究:(已知碱石灰是NaOH和CaO的混合物,常用于干燥、吸收气体)
①该实验若不用碱石灰,则所测得的粗锌中锌的质量分数将 (填“偏大”、“偏小”或“无影响”);
②若将粗锌换成某含有杂质的石灰石样品(杂质也不与稀盐酸反应),判断该实验方案能不能用于石灰石样品中CaCO3质量分数的测定,并说明理由____________________。
练习册系列答案
相关题目
17.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液中提取乙醇 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
14.下列叙述中正确的是( )
| A. | 离子晶体中肯定不含非极性共价键 | B. | 原子晶体的熔点肯定高于其他晶体 | ||
| C. | 由分子组成的物质其熔点一定较低 | D. | 构成晶体的粒子一定含有共价键 |
1.硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.其部分性质如下表:
回答下列问题:
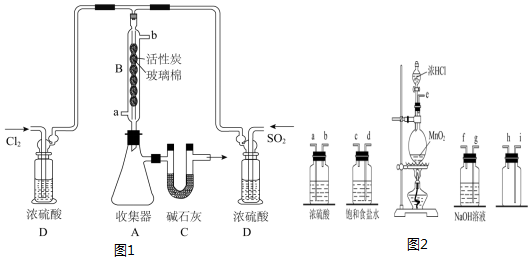
I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑ |

I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
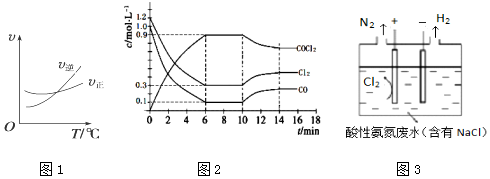
2.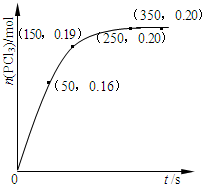 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% | |
| D. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |
18.Ⅰ.氮的固定是几百年来科学家一直研究的课题.
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
①分析数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.
②分析数据可知;人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
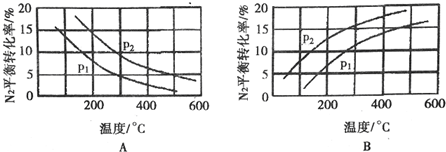
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较p1、p2的大小关系:p2>pl.
Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1=60%.
②已知平衡时,容器压强为8MPa,则平衡常数Kp=0.26 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮N2(g)+O2(g)?2NO(g) | 工业固氮N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.8×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知;人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较p1、p2的大小关系:p2>pl.

Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol.
①达平衡时,H2的转化率α1=60%.
②已知平衡时,容器压强为8MPa,则平衡常数Kp=0.26 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
19. 某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且半分钟不恢复原色,立即停止滴定.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D、E(填序号).
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如图所示.则起始读数为V1=9.00mL,终点读数V2=26.10mL.
(4)再结合表数据,计算被测氢氧化钠溶液的物质的量浓度是0.1710mol•L-1.
 某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某同学欲用已知物质的量浓度为0.100 0mol•L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且半分钟不恢复原色,立即停止滴定.
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D、E(填序号).
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若第一次滴定开始和结束时,酸式滴定管中的液面如图所示.则起始读数为V1=9.00mL,终点读数V2=26.10mL.
(4)再结合表数据,计算被测氢氧化钠溶液的物质的量浓度是0.1710mol•L-1.
| 滴定 | 待测溶液 体积/mL | 标准酸体积 | |
| 滴定前的刻度/mL | 滴定后的刻度/mL | ||
| 第一次 | 10.00 | V1 | V2 |
| 第二次 | 10.00 | 4.10 | 21.10 |
| 第三次 | 10.00 | 0.40 | 17.60 |


 B.
B.  C.
C.  D.
D.