题目内容
2.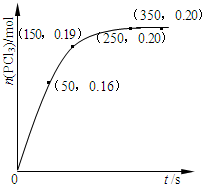 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% | |
| D. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |
分析 A.由图中数据可知50s内,△n(PCl3)=0.16mol,根据v=$\frac{△c}{△t}$计算v(PCl3);
B.由图中数据可知,平衡时n(PCl3)=0.2mol,保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol/L,则n′(PCl3)=0.22mol>0.2mol,说明升高温度平衡向正反应方向移动,升高温度平衡向吸热反应方向移动;
C.等效为起始加入2.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动,平衡时的PCl5转化率较原平衡低,故平衡时PCl3的物质的量小于0.4mol,即相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,参加反应的PCl3的物质的量大于1.6mol;
D.先计算平衡常数K,再计算浓度商(Qc),K>Qc,说明平衡向正反应方向移动,K<Qc,说明平衡向逆反应方向移动,K=Qc,说明平衡不移动,据此判断平衡移动方向,进而判断反应达到平衡前v(正)、v(逆)相对大小.
解答 解:A.由图中数据可知50s内,△n(PCl3)=0.16mol,v(PCl3)=$\frac{△c}{△t}$=$\frac{0.16mol}{\frac{2L}{50s}}$=0.0016mol/(L•s),故A错误;
B.由图中数据可知,平衡时n(PCl3)=0.2mol,保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol/L,则n′(PCl3)=0.11 mol/L×2L=0.22mol>0.2mol,说明升高温度平衡正向移动,升高温度平衡向吸热反应方向移动,故正反应为吸热反应,即△H>O,故B错误;
C.等效为起始加入2.0molPCl5,与原平衡相比,压强增大,平衡向逆反应方向移动,平衡时的PCl5转化率较原平衡低,故平衡时PCl3的物质的量小于0.4mol,即相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,参加反应的PCl3的物质的量大于1.6mol,故达到平衡时,PCl3的转化率高于$\frac{1.6mol}{2mol}$=80%,故C错误;
D.起始时PCl5的浓度为0.5mol/L,由图可知,平衡时PCl3的浓度为$\frac{0.2mol}{2L}$=0.1mol/L,则:
PCl5(g)?PCl3(g)+Cl2(g)
开始(mol/L):0.5 0 0
变化(mol/L):0.1 0.1 0.1
平衡(mol/L):0.4 0.1 0.1
所以平衡常数K=$\frac{0.1×0.1}{0.4}$=0.025,
起始时向容器中充入1.0 mol PCl5、0.20 molPCl3和0.20 molCl2,起始时PCl5的浓度为0.5mol/L、PCl3的浓度为0.1mol/L、Cl2的浓度为0.1mol/L,浓度商Qc=$\frac{0.1×0.1}{0.5}$=0.02<K=0.025,说明平衡向正反应方向移动,反应达平衡前v(正)>v(逆),故D正确;
故选D.
点评 本题考查物质的量随时间变化曲线、反应速率计算、平衡常数应用、等效平衡等,注意C中利用等效平衡思想分析,使问题简单化,也可以根据平衡常数计算,相对繁琐,注意理解根据浓度商与平衡常数关系判断反应进行方向,题目难度中等.

| A. | 我国目前最主要的能源是煤炭 | |
| B. | 人体运动所消耗的能量与化学反应无关 | |
| C. | 人类目前所直接利用的能量大部分是由化学反应所产生的 | |
| D. | 煤、石油、天然气是当今世界最重要的三种化石燃料 |
| A. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| B. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 实验室金属钠着火,立即用水浇灭 |
| A. | S$\stackrel{O_{2}/点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | NH3$→_{催化剂,△}^{O_{2}}$N2$\stackrel{O_{2},H_{2}O}{→}$HNO3 | |
| C. | SiO2$\stackrel{C/高温}{→}$Si$\stackrel{Cl_{2}、高温}{→}$SiCl4$\stackrel{H_{2}、高温}{→}$Si | |
| D. | 海水$\stackrel{熟石灰}{→}$Mg(OH)2 $\stackrel{电解}{→}$Mg |
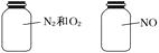
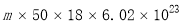 B.
B.
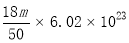 D.
D.