题目内容
一定量的盐酸跟过量的铁粉反应时,为了减缓反应的速率,且不影响生成H2的总量,可向反应容器中加入适量的( )
| A、氢氧化钠固体 |
| B、硝酸钠溶液 |
| C、硫酸钾溶液 |
| D、碳酸钠固体 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:因Fe过量,则减小氢离子的浓度,不改变氢离子的物质的量,可满足减缓反应速率但又不影响生成H2的总量,以此来解答.
解答:
解:A.NaOH与酸中和,引起H+离子的物质的量的减小,浓度减小,反应速率减慢,但氢气的总量也在减少,故A错误;
B.加入NaNO3溶液,生成NO气体,不生成氢气,故B错误;
C.加入K2SO4溶液,H+浓度降低,但总量不变,可减缓反应速率且不影响生成H2的总量,故C正确;
D.因盐酸与Na2CO3固体反应,会导致生成氢气的量减少,故D错误;
故选C.
B.加入NaNO3溶液,生成NO气体,不生成氢气,故B错误;
C.加入K2SO4溶液,H+浓度降低,但总量不变,可减缓反应速率且不影响生成H2的总量,故C正确;
D.因盐酸与Na2CO3固体反应,会导致生成氢气的量减少,故D错误;
故选C.
点评:本题考查影响化学反应速率的因素,注意氢离子的浓度变小而与铁反应的氢离子总物质的量不变是解答本题的关键,并熟悉物质之间的反应来解答,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知25℃时有关弱酸的电离平衡常数:
由此可得出( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A、对应钠盐溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |
| B、CO2通入NaCN溶液中有:CO2+H2O+2NaCN→Na2CO3+2HCN |
| C、冰醋酸中逐滴加水,溶液的导电性、pH均先增大后减小 |
| D、NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
研究物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能量变化.据此判断以下叙述中错误的是( )
| A、金属钠与氯气反应生成氯化钠后,稳定性增强,体系的能量降低 |
| B、物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来 |
| C、氮分子内部存在着很强的共价键,故通常状况下氮气的化学性质很不活泼 |
| D、需加热才能发生的反应一定是吸收能量的反应 |
下列关于化学反应和能量变化关系的描述中,说法不正确的是( )
| A、放热反应,不必加热就一定能发生 |
| B、化学反应中一定有能量变化 |
| C、吸热反应不一定需要加热也能发生 |
| D、热化学方程式中,热效应数值与反应物的物质的量多少有关 |
下列反应中,属于氧化还原反应同时又是吸热反应的是( )
| A、Ba(OH)2?8H2O与NH4Cl反应 |
| B、铝与稀盐酸 |
| C、灼热的炭与水蒸气生成一氧化碳和氢气的反应 |
| D、煤与O2的燃烧反应 |
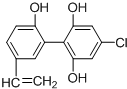 在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )
在2010年温哥华冬季奥运会上,有个别运动员因服用兴奋剂被取消参赛的资格.如图是检测出兴奋剂的某种同系物X的结构,关于X的说法正确的是( )| A、X分子中不可能所有原子都在同一平面上 |
| B、X遇到FeCl3溶液时显紫色,而且能使溴的四氯化碳溶液褪色 |
| C、1mol X与足量的浓溴水反应,最多消耗5mol Br2 |
| D、1mol X在一定条件下与足量的氢气反应,最多消耗1mol H2 |