题目内容
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
| A、1.5mL | B、2.4mL |
| C、3.6mL | D、4mL |
考点:有关混合物反应的计算
专题:计算题
分析:NO2和O2混合气体与反应可能的反应式有:4NO2+O2+2H2O=4HNO3、3NO2+H2O=2HNO3+NO,根据反应的方程式有讨论的方法计算.
解答:
解:若氧气过量,则剩余2mL无色气体为氧气,设参加反应的氧气的体积为x,则有:
4NO2+O2+2H2O=4HNO3
4x x
4x+x=12mL-2mL=10mL,
解得:x=2mL,
原混合气体中氧气的体积为:2mL+2mL=4mL;
若NO2过量,则剩余2mL无色气体为NO,设氧气的体积为y,
4NO2+O2+2H2O=4HNO3
4y y
3NO2+H2O=2HNO3+NO
3 1
(12mL-y-4y) 2mL
解得:y=1.2mL,即:原混合物中含有1.2mL氧气,
故选D.
4NO2+O2+2H2O=4HNO3
4x x
4x+x=12mL-2mL=10mL,
解得:x=2mL,
原混合气体中氧气的体积为:2mL+2mL=4mL;
若NO2过量,则剩余2mL无色气体为NO,设氧气的体积为y,
4NO2+O2+2H2O=4HNO3
4y y
3NO2+H2O=2HNO3+NO
3 1
(12mL-y-4y) 2mL
解得:y=1.2mL,即:原混合物中含有1.2mL氧气,
故选D.
点评:本题考查混合物的计算,题目难度中等,注意气体的过量判断,明确讨论法在化学计算中的应用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
常温时,下列各组离子在指定溶液中,能大量共存的是( )
| A、pH=11的溶液中:Na+、[Al(OH)4]-、S2-、SO32- |
| B、水电离的浓度为 10-12mol?L-1的溶液中:Cl-、CO32-、NH4+、SO32- |
| C、使石蕊变红的溶液中:Fe2+、MnO4-、Na+、SO42- |
| D、中性溶液中:Fe3+、Al3+、I-、S2- |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、32g O3所含有的原子数为2NA |
| B、18g NH4+中所含的离子数为NA |
| C、22.4LCO2所含的原子数为3NA |
| D、1 mol/L碳酸钠溶液中所含钠离子的总数为2 NA |
常温下,下列有关醋酸的叙述中不正确的是( )
| A、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B、将pH=a的醋酸稀释为pH=a+1的过程中,c(OH-)不断增大 |
| C、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
| D、浓度均为0.1 mol-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
如表是周期表中短周期的一部分,已知B与C的原子序数之和是A原子序数的4倍,则下列说法中正确的是( )
| A | ||
| C | B |
| A、A元素的最高正价为+6价 |
| B、A、B、C依次是氧、氯、磷 |
| C、B元素的单质常温下是一种黄绿色气体 |
| D、C单质常用来制作计算机的芯片 |
已知:
C(石墨)+O2(g)=CO2(g)△H1; H2(g)+
O2(g)=H2O(1)△H2
CH3CH2OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H3
2C(石墨)+
O2(g)+3H2(g)=CH3CH2OH(1)△H4
下列关于上述反应焓变的判断正确的是( )
C(石墨)+O2(g)=CO2(g)△H1; H2(g)+
| 1 |
| 2 |
CH3CH2OH(1)+3O2(g)=2CO2(g)+3H2O(1)△H3
2C(石墨)+
| 1 |
| 2 |
下列关于上述反应焓变的判断正确的是( )
| A、△H1>0,△H3<0 |
| B、△H2>0,△H4>0 |
| C、△H4=△H1+△H2-△H3 |
| D、△H3=2△H1+3△H2-△H4 |

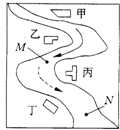 某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现四个工厂,如右图所示.这些厂往小河里排放的废水中各含一种化合物.经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成;⑥N处水样的pH小于7.请回答:
某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现四个工厂,如右图所示.这些厂往小河里排放的废水中各含一种化合物.经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成;⑥N处水样的pH小于7.请回答: