题目内容
T℃时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )


| A、平衡时X、Y的转化率相同 |
| B、该反应的化学方程式为:X(g)+Y(g)?2Z(g) |
| C、T℃时,若起始时X为2.00 mol,Y为2.00 mol,达平衡时Y的体积分数与原平衡Y的体积分数相同 |
| D、达到平衡后,将容器体积扩大为4L,平衡向逆反应方向移动 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:根据图象知,反应物为X、Y,生成物为Z,0-10s时,反应物X物质的量减少(1.20-0.40)mol=0.80mol,Y的物质的量减少(1.00-0.20)mol=0.80mol,Z的物质的量增加1.60mol.
A.X、Y的起始物质的量之比不等于化学计量数之比,二者转化率一定不相等;
B.参加反应的X、Y、Z的物质的量之比=0.80mol:0.80mol:1.60mol=1:1:2,所以该反应方程式为x(g)+Y(g)?2Z(g);
C.T℃时,若起始时X为2.00 mol,Y为2.00 mol,相当在在原平衡的基础上增加Y;
D.该反应为气体体积不变的反应,改变压强不平衡移动;
A.X、Y的起始物质的量之比不等于化学计量数之比,二者转化率一定不相等;
B.参加反应的X、Y、Z的物质的量之比=0.80mol:0.80mol:1.60mol=1:1:2,所以该反应方程式为x(g)+Y(g)?2Z(g);
C.T℃时,若起始时X为2.00 mol,Y为2.00 mol,相当在在原平衡的基础上增加Y;
D.该反应为气体体积不变的反应,改变压强不平衡移动;
解答:
解:根据图象知,反应物为X、Y,生成物为Z,0-10s时,反应物X物质的量减少(1.20-0.40)mol=0.80mol,Y的物质的量减少(1.00-0.20)mol=0.80mol,Z的物质的量增加1.60mol.
A.X、Y的起始物质的量之比不等于化学计量数之比,二者转化率一定不相等,故A错误;
B.参加反应的X、Y、Z的物质的量之比=0.80mol:0.80mol:1.60mol=1:1:2,所以该反应方程式为x(g)+Y(g)?2Z(g),故B正确;
C.T℃时,若起始时X为2.00 mol,Y为2.00 mol,相当在在原平衡的基础上增加Y,达平衡时Y的体积分数增大,故C错误;
D.该反应为气体体积不变的反应,改变压强不平衡移动,故D错误;
故选B.
A.X、Y的起始物质的量之比不等于化学计量数之比,二者转化率一定不相等,故A错误;
B.参加反应的X、Y、Z的物质的量之比=0.80mol:0.80mol:1.60mol=1:1:2,所以该反应方程式为x(g)+Y(g)?2Z(g),故B正确;
C.T℃时,若起始时X为2.00 mol,Y为2.00 mol,相当在在原平衡的基础上增加Y,达平衡时Y的体积分数增大,故C错误;
D.该反应为气体体积不变的反应,改变压强不平衡移动,故D错误;
故选B.
点评:本题考查化学平衡图象问题,涉及化学平衡有关计算、平衡常数、影响化学平衡的因素等,题目难度不大,注意分析图象中各物理量的变化曲线,书写方程式是解题关键.

练习册系列答案
相关题目
某物质经分析知,其中仅含一种元素,此物质( )
| A、一定是一种单质 |
| B、可能是纯净物也可能是混合物 |
| C、一定是纯净物 |
| D、可能是单质也可能是化合物 |
下列反应中生成物总能量高于反应物总能量的是( )
| A、碳酸钙受热分解 |
| B、乙醇燃烧 |
| C、氧化钙溶于水 |
| D、铝粉与氧化铁粉末混合加热反应 |
下列说法正确的是( )
| A、纤维素、淀粉、蛋白质、油脂在一定条件下都能发生水解反应 |
B、向肉桂醛(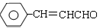 )中滴加酸性高锰酸钾溶液,紫红色很快褪去,此现象可用来证明肉桂醛分子中一定含有醛基 )中滴加酸性高锰酸钾溶液,紫红色很快褪去,此现象可用来证明肉桂醛分子中一定含有醛基 |
| C、亚硫酸氢钠可作为药物用来治疗胃溃疡病人的胃酸过多症 |
| D、铝箔和金箔置于冷的浓硫酸中均无明显现象,两者原理相同 |
通常状况下,NC13是一种油状液体,其分子空间构型与氨分子相似,下列对NC13的有关叙述正确的是( )
| A、分子中N-C1键键长比CCl4分子中C-C1键键长长 |
| B、分子中的所有原于均达到8电子稳定结构 |
| C、NCl3分子是非极性分子 |
| D、NBr3比NCl3易挥发 |
下列关于晶体的说法正确的是( )
| A、构成分子晶体的微粒之间可能含有离子键 |
| B、原子晶体一定是单质 |
| C、离子晶体熔化时,需要克服离子键 |
| D、碘晶体升华时,分子中共价键发生断裂 |
下列事实的解释正确的是( )
| A、将SO2、SO3 混合气体通入氯化钡溶液中,出现浑浊是因为生成了BaSO4沉淀 | ||||
| B、SO2通入溴水中,溴水褪色,是因为SO2的漂白性 | ||||
C、反应2C+SiO2
| ||||
| D、在NaHCO3的溶液中滴加NaAlO2溶液中有白色沉淀生成,是因为二者发生完全水解反应 |
某温度下,碳和水在密闭容器中发生下列反应:C(s)+H2O(g)?CO(g)+H2,CO(g)+H2O(g)?CO2(g)+H2当反应达平衡时,测得c(H2)=1.9mol/L,c(CO2)=0.9mol/L,则CO的浓度为( )
| A、0.1mol/L |
| B、0.9mol/L |
| C、1.8mol/L |
| D、1.9mol/L |