题目内容
12.下列实验操作能达到目的是( )①用Na2S溶液和Al2(SO4)3溶液混合反应制取Al2S3固体
②用加热蒸发K2CO3溶液的方法获得KOH晶体
③除去MgCl2溶液中混有的少量FeCl3,可加入足量的Mg(OH)2粉末搅拌后过滤
④室温下,pH=5的NaHSO4溶液中水的电离程度等于pH=9的氨水中水的电离程度.
| A. | ①② | B. | ①③ | C. | ③④ | D. | ②③ |
分析 ①Na2S溶液和Al2(SO4)3溶液,相互促进水解生成氢氧化铝;
②加热蒸发K2CO3溶液,最终为碳酸钾;
③Mg(OH)2粉末可促进铁离子水解转化为沉淀;
④pH=5的NaHSO4溶液电离出氢离子浓度等于pH=9的氨水中电离出氢氧根离子浓度,均抑制水的电离.
解答 解:①Na2S溶液和Al2(SO4)3溶液,相互促进水解生成氢氧化铝,不能发生复分解反应生成Al2S3固体,故错误;
②加热蒸发K2CO3溶液,最终为碳酸钾,不能得到KOH,故错误;
③Mg(OH)2粉末可促进铁离子水解转化为沉淀,则过滤可除杂,故正确;
④pH=5的NaHSO4溶液电离出氢离子浓度等于pH=9的氨水中电离出氢氧根离子浓度,均抑制水的电离,则水的电离程度相同,故正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握盐类水解、弱电解质的电离、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
3.下列物质属于醇类的是( )
| A. | 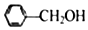 | B. | 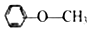 | C. | 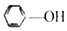 | D. | 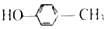 |
7.在如图所示的装置中,a的金属活动性比氢强,b为碳棒,关于此装置的各种叙述不正确的是( )

| A. | 碳棒上有气体放出,溶液pH变大 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电子从a极流向b极 | |
| D. | a极上发生了氧化反应 |
17.NA为阿伏伽徳罗常数的值,下列说法不正确的是( )
| A. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| B. | 常温常压下的67.2L氯气与27g铝充分反应,转移电子数为3NA | |
| C. | 1L 1mol/L的稀硝酸中,含氧原子数为3NA | |
| D. | 1molCO和CO2混合气体中含C原子数为NA |
4.将某一元弱酸(HA)和氢氧化钠溶液混合,所得溶液呈中性,则此溶液中c(Na+)与c(A-)的大小关系为( )
| A. | c(Na+)=c(A-) | B. | c(Na+)<c(A-) | C. | c(Na+)>c(A-) | D. | 无法确定 |
