题目内容
4.将某一元弱酸(HA)和氢氧化钠溶液混合,所得溶液呈中性,则此溶液中c(Na+)与c(A-)的大小关系为( )| A. | c(Na+)=c(A-) | B. | c(Na+)<c(A-) | C. | c(Na+)>c(A-) | D. | 无法确定 |
分析 某一元弱酸(HA)和氢氧化钠溶液混合,所得溶液呈中性,可知c(H+)=c(OH-),结合电荷守恒判断c(Na+)与c(A-)的大小关系.
解答 解:某一元弱酸(HA)和氢氧化钠溶液混合,溶液遵循电荷守恒,则电荷守恒式为c(H+)+c(Na+)=c(A-)+c(OH-),
所得溶液呈中性,可知c(H+)=c(OH-),则c(Na+)=c(A-),
故选A.
点评 本题考查离子浓度的比较,为高频考点,把握溶液中电荷守恒式、中性为解答的关键,侧重分析与应用能力的考查,注意电荷守恒的应用,题目难度不大.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
14.下列各组离子能够在指定的环境下大量共存的是( )
| A. | 在pH=1的溶液中:Na+、K+、MnO4-、S2O32- | |
| B. | 和Al反应能产生氢气的溶液:K+、NH4+、Cl-、S2- | |
| C. | 中性溶液:Al3+、K+、SO42-、AlO2- | |
| D. | c(H+)<c(OH-)的溶液:Na+、K+、SO42-、S2- |
15.已知Na2SO3溶液可与K2Cr2O7溶液反应,现有0.1mol/L的Na2SO3溶液12mL,恰好与0.04mol/L的K2Cr2O7溶液10mL完全反应,通过计算确定Cr元素在还原产物中的化合价( )
| A. | +1 | B. | +3 | C. | +4 | D. | +5 |
19.下列除去杂质(括号内的物质为杂质)的方法中错误的是( )
| A. | FeSO4 (CuSO4):加足量铁粉后,过滤 | |
| B. | CO (CO2):用NaOH溶液洗气后干燥 | |
| C. | CO2 (HCl):用NaOH溶液洗气后干燥 | |
| D. | MnO2 (KCl):加水溶解后,过滤、洗涤、烘干 |
16.下列表格中各项分类都正确的一组是( )
| 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 纯碱 | 冰水混合物 | 液态KNO3 | 蔗糖 |
| B | CaO | 海水 | 铜 | 乙醇 |
| C | 明矾 | 铝合金 | AgCl | CO2 |
| D | 氢氧化钠 | 空气 | 氨水 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
13.甲、乙、丙、丁分别是BaCl2、NaOH、FeCl2、Al2(SO4)3、四种物质中的一种.若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生.据此可推断丙物质是( )
| A. | BaCl2 | B. | NaOH | C. | FeCl2 | D. | Al2(SO4)3 |
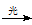 CH3Cl+HCl
CH3Cl+HCl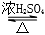 CH3COOCH2CH33+H2O
CH3COOCH2CH33+H2O 2CH3CHO+2H2O
2CH3CHO+2H2O