题目内容
12.现有①、②、③三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4; ②1s22s22p63s23p3; ③1s22s22p5.则下列有关比较中正确的是( )
| A. | 第一电离能:③>②>① | B. | 原子半径:①>②>③ | ||
| C. | 电负性:③>②>① | D. | 最高正化合价:③>①>② |
分析 由核外电子排布式可知,①1s22s22p63s23p4为S元素,②1s22s22p63s23p3为P元素,③1s22s22p5为F元素.
A.同周期随原子序数增大,元素第一电离能呈增大趋势,P元素原子3p能级为半满稳定状态,第一电离能高于同周期相邻元素,同主族自上而下第一电离能减小;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大;
C.同周期自左而右电负性增大,同主族自上而下电负性减小;
D.最高正化合价等于最外层电子数,注意F、O元素一般没有正化合价.
解答 解:由核外电子排布式可知,①1s22s22p63s23p4为S元素,②1s22s22p63s23p3为P元素,③1s22s22p5为F元素.
A.同周期随原子序数增大,元素第一电离能呈增大趋势,P元素原子3p能级为半满稳定状态,第一电离能高于同周期相邻元素,同主族自上而下第一电离能减小,故第一电离能F>P>S,即③>②>①,故A正确;
B.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径P>S>F,即②>①>③,故B错误;
C.同周期自左而右电负性增大,同主族自上而下电负性减小,故电负性③>①>②,故C错误;
D.S元素最高正化合价为+6,P元素最高正化合价为+5,故最高正化合价:①>②,但F没有正化合价,故D错误.
故选:A.
点评 本题考查核外电子排布规律、元素周期律等,难度不大,注意能级处于半满、全满时元素的第一电离能高于同周期相邻元素.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
9.糖尿病患者的尿液中含有葡萄糖,而且病情越重,含糖量越高,所以,从前在医疗上把氢氧化钠和硫酸铜溶液加入病人的尿液中,加热后通过观察是否有红色沉淀来判断病情,请分析,以下哪些药品和新制Cu(0H)2共热会有类似的现象( )
①淀粉 ②福尔马林 ③纤维素 ④蚁酸 ⑤甲酸乙酯 ⑥乙酸甲酯 ⑦甲酸钠 ⑧蔗糖 ⑨白酒 ⑩食醋⑪麦芽糖.
①淀粉 ②福尔马林 ③纤维素 ④蚁酸 ⑤甲酸乙酯 ⑥乙酸甲酯 ⑦甲酸钠 ⑧蔗糖 ⑨白酒 ⑩食醋⑪麦芽糖.
| A. | 全部 | B. | ①③④⑤⑨ | C. | ②④⑤⑦⑪ | D. | ②④⑤⑥⑦⑧ |
3.已知化学反应①:
Fe(s)+CO2(g)═FeO(s)+CO(g),其平衡常数为K1;化学反应②:
Fe(s)+H2O(g)═FeO(s)+H2(g),其平衡常数为K2.在温度
973K和1173K情况下,K1、K2的值分别如下:
(1)通过表格中的数值可以推断:反应①是吸热(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式及上表数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有DF(填写序号).
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
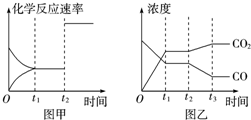
(4)图甲、乙分别表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是加入催化剂或增大体系的压强.
②图乙中t2时刻发生改变的条件是降低温度或增加水蒸气的量或减少氢气的量.
Fe(s)+CO2(g)═FeO(s)+CO(g),其平衡常数为K1;化学反应②:
Fe(s)+H2O(g)═FeO(s)+H2(g),其平衡常数为K2.在温度
973K和1173K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)=CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式及上表数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应,要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有DF(填写序号).
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量
(4)图甲、乙分别表示反应③在t1时刻达到平衡、在t2时刻因改变某个条件而发生变化的情况:
①图甲中t2时刻发生改变的条件是加入催化剂或增大体系的压强.
②图乙中t2时刻发生改变的条件是降低温度或增加水蒸气的量或减少氢气的量.

20.在下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | NaCl | D. | MgSO4 |
7.下列关于物质性质的说法不正确的是( )
| A. | 通常状况下,NO2是红棕色的气体 | |
| B. | 氯水光照久置后最终变为稀盐酸 | |
| C. | 氯化钙溶液和AgNO3溶液混合有白色沉淀产生 | |
| D. | 加热时,铁单质与浓硝酸不发生反应 |
 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题: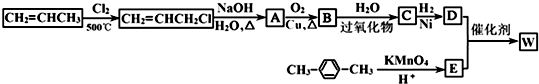
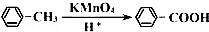
 .
.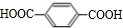 →
→ +2H2O.
+2H2O. .
. .
.