题目内容
 mA(g)+nB(g)?pC(g)△H<0,室温条件下,在一容积不变的密闭容器中加入一定量的A、B,B%与压强(P)的关系如图所示,则下列有关叙述正确的是( )
mA(g)+nB(g)?pC(g)△H<0,室温条件下,在一容积不变的密闭容器中加入一定量的A、B,B%与压强(P)的关系如图所示,则下列有关叙述正确的是( )| A、m+n>p |
| B、n>p |
| C、X点时混合物的正反应速率小于逆反应速率 |
| D、X点比Y点混合物的反应速率慢 |
考点:体积百分含量随温度、压强变化曲线
专题:
分析:曲线上的点都是平衡点,由图可知,压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动;
x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,
y点B的百分含量低于相同压强平衡点的含量,说明y点未到达平衡状态,反应向逆反应移动,据此结合选项解答.
x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,
y点B的百分含量低于相同压强平衡点的含量,说明y点未到达平衡状态,反应向逆反应移动,据此结合选项解答.
解答:
解:曲线上的点都是平衡点,由图可知,压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动;
x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,
y点B的百分含量低于相同压强平衡点的含量,说明y点未到达平衡状态,反应向逆反应移动,
A、压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动,故m+n<p,故A错误;
B、压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动,故m+n<p,故B错误;
C、x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,所以正反应速率大于逆反应速率,故C错误;
D、X点比Y点的压强小,所以X点比Y点混合物的反应速率慢,故D正确;
故选D.
x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,
y点B的百分含量低于相同压强平衡点的含量,说明y点未到达平衡状态,反应向逆反应移动,
A、压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动,故m+n<p,故A错误;
B、压强越大,B的百分含量越高,说明增大压强平衡向逆反应移动,故m+n<p,故B错误;
C、x点B的百分含量高于相同压强平衡点的含量,说明x点未到达平衡状态,反应向正反应移动,所以正反应速率大于逆反应速率,故C错误;
D、X点比Y点的压强小,所以X点比Y点混合物的反应速率慢,故D正确;
故选D.
点评:本题考查化学平衡图象、化学平衡移动的影响因素等,难度中等,注意根据B的含量判断反应进行的方向.

练习册系列答案
相关题目
食品卫生与身体健康密切相关,下列做法对人体有害的是( )
①香肠中添加过量的亚硝酸钠;
②烧鱼时加点食醋;
③白酒中掺入工业酒精;
④食品原料中添加“苏丹红一号“
①香肠中添加过量的亚硝酸钠;
②烧鱼时加点食醋;
③白酒中掺入工业酒精;
④食品原料中添加“苏丹红一号“
| A、①②③ | B、①③④ |
| C、②③④ | D、①②③④ |
为了除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入(已知Fe(OH)3只要在pH>4的环境里就可以沉淀完全)( )
| A、NaOH |
| B、Na2CO3 |
| C、氨水 |
| D、MgO |
25℃时,下列溶液中,离子浓度关系正确的是( )
| A、pH=a的氨水稀释10倍后,其pH=b,则a=b+1 |
| B、浓度相同的①NH4Cl ②CH3COONH4③NH4HSO4,三种溶液中的c(NH4+):①>③>② |
| C、将相同浓度的氨水与盐酸等体积混合,所得溶液中的离子浓度关系:c (NH4+)>c (Cl-)>c (H+)>c (OH-) |
| D、将a mol?L-1CH3COOH与b mol?L-1NaOH溶液等体积混合,测得溶液pH为7,则a与b的关系:a>b |
在恒温恒容的密闭容器中,可逆反应2SO2(g)+O2(g)?2SO3(g),下列判断不正确的是( )
| A、达到化学平衡时,2v正(O2)=v逆(SO3) |
| B、达到化学平衡时,容器中气体压强不再变化 |
| C、若单位时间内生成xmolSO3的同时消耗xmolSO2,则反应达到平衡状态 |
| D、达到化学平衡时,容器中混合气体的平均相对分子质量不再变化 |
现有三种元素的基态原子的电子排布式如下:①[Ne]3s23p4;②1s22s22p63s23p3;③1s22s22p5.则上述三种原子的第一电离能大小关系正确的是( )
| A、②>①>③ |
| B、③>①>② |
| C、③>②>① |
| D、①>②>③ |
下列有关物质性质的描述和该性质的应用均正确的是( )
| A、氨气具有氧化性,用浓氨水检验氯气管道是否泄漏 |
| B、金属镁着火可用干粉灭火器灭火,也可用泡沫灭火器灭火 |
| C、二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气 |
| D、铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
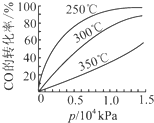 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.