题目内容
20.下列物质属于纯净物的是( )| A. | 碘酒 | B. | 漂白粉 | C. | 食盐水 | D. | 液氯 |
分析 纯净物是同种物质组成的,不同物质组成的为混合物,宏观上只含一种物质的为纯净物,微观上是只含一种分子的为纯净物,纯净物依据组成元素分为单质和化合物;
解答 解:A.碘酒是碘单质溶解在酒精中形成的溶液分散系,是混合物,故A错误;
B.漂白粉是氯化钙和次氯酸钙组成的混合物,故B错误;
C.食盐水是氯化钠的水溶液,属于溶液分散系,是混合物,故C错误;
D.液氯是一种物质组成的纯净物,是氯元素的单质,故D正确;
故选D.
点评 本题考查了物质分类、物质组成、物质名称的分析判断,掌握概念实质是解题关键,题目较简单.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
11.下列关于元素周期律的说法中错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 离子的还原性:S2->Cl->Br->I- | |
| C. | 酸性:H2SO4>H3PO4>H2CO3>HClO | |
| D. | 金属性:Be<Mg<Ca<K |
8.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 任何放热反应在常温条件下一定能自发进行 | |
| C. | 反应物和生成物所具有的总焓决定了反应是放热还是吸热 | |
| D. | 放热反应在任何条件下也能发生反应 |
5.下列反应的离子方程式表示正确的是( )
| A. | 澄清石灰水中通入过量二氧化碳:OH-+CO2═HCO3- | |
| B. | 向水玻璃中中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
12.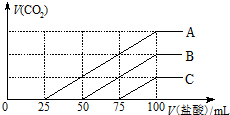 浓度相同的NaOH溶液各100ml 倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐渐加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示.下列判断正确的是( )
浓度相同的NaOH溶液各100ml 倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐渐加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示.下列判断正确的是( )
 浓度相同的NaOH溶液各100ml 倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐渐加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示.下列判断正确的是( )
浓度相同的NaOH溶液各100ml 倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐渐加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示.下列判断正确的是( )| A. | 原NaOH溶液的浓度为0.2mol/L | |
| B. | B烧杯中通入CO2体积为448ml | |
| C. | 通入CO2后,不能确定A烧杯中的溶质 | |
| D. | 通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=2:1 |
10.下列溶液中c(Cl-)与50mL1mol•L-1的AlCl3溶液中c(Cl-)相等的是( )
| A. | 150mL1mol•L-1NaCl溶液 | B. | 75mL2mol•L-1CaCl2溶液 | ||
| C. | 150mL3mol•L-1KCl溶液 | D. | 75mL3mol•L-1FeCl3溶液 |