题目内容
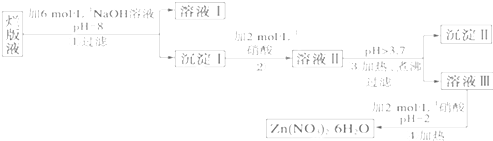
气体A的产量是衡量一个国家石油化工发展水平的标志,D是食醋的主要成分.A能发生以下转化.

(1)A结构简式 ;F结构简式 ;
(2)指出下列反应的反应类型① ; ③ ;
(3)写出下列反应的化学方程式② ,④ .

(1)A结构简式
(2)指出下列反应的反应类型①
(3)写出下列反应的化学方程式②
考点:有机物的推断
专题:有机物的化学性质及推断
分析:气体A的产量是衡量一个国家石油化工发展水平的标志,则A是乙烯,D是食醋中的主要成分则D是乙酸,乙烯和水发生加成反应生成B是乙醇,乙醇发生氧化反应生成C为乙醛,乙醛进一步发生氧化反应生成乙酸,乙醇和乙酸发生酯化反应生成F是乙酸乙酯,乙烯与HCl发生和加成反应生成E是氯乙烷,据此解答.
解答:
解:气体A的产量是衡量一个国家石油化工发展水平的标志,则A是乙烯,D是食醋中的主要成分则D是乙酸,乙烯和水发生加成反应生成B是乙醇,乙醇发生氧化反应生成C为乙醛,乙醛进一步发生氧化反应生成乙酸,乙醇和乙酸发生酯化反应生成F是乙酸乙酯,乙烯与HCl发生和加成反应生成E是氯乙烷,
(1)A是乙烯,含有碳碳双键,结构简式为CH2=CH2,F是乙酸乙酯,结构简式为CH3COOCH2CH3,故答案为:CH2=CH2;CH3COOCH2CH3;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应 ③是乙酸与乙醇发生酯化反应生成乙酸乙酯,也属于取代反应,故答案为:加成反应;酯化反应或取代反应;
(3)反应②是乙醇氧化生成乙醛,反应化学方程式为:2CH3CH2OH+O2
2CH3CHO+H2O,反应④是乙烯与HCl发生加成反应生成氯乙烷,反应方程式为:CH2=CH2+HCl
CH3CH2Cl,
故答案为:2CH3CH2OH+O2
2CH3CHO+H2O;CH2=CH2+HCl
CH3CH2Cl.
(1)A是乙烯,含有碳碳双键,结构简式为CH2=CH2,F是乙酸乙酯,结构简式为CH3COOCH2CH3,故答案为:CH2=CH2;CH3COOCH2CH3;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应 ③是乙酸与乙醇发生酯化反应生成乙酸乙酯,也属于取代反应,故答案为:加成反应;酯化反应或取代反应;
(3)反应②是乙醇氧化生成乙醛,反应化学方程式为:2CH3CH2OH+O2
| Cu |
| △ |
| 催化剂 |
故答案为:2CH3CH2OH+O2
| Cu |
| △ |
| 催化剂 |
点评:本题考查有机物的推断,涉及烯烃、醇、醛、羧酸、酯的性质与转化,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
下列关于科学家及其提出学说与贡献的叙述不对应的是( )
| A、道尔顿提出原子学说 |
| B、汤姆生发现电子,并提出原子结构轨道模型 |
| C、舍勒发现了氯气 |
| D、卢瑟福根据α粒子散射现象,提出了带核的原子结构模型 |
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的热稳定性c>d,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是( )
| A、b、a、e、d、c |
| B、e、b、a、d、c |
| C、b、a、d、c、e |
| D、c、d、e、a、b |
能在水溶液中大量共存的一组离子是( )
| A、K+、H+、NO3-、SiO32- |
| B、H+、NH4+、Al3+、SO42- |
| C、Fe2+、H+、ClO-、SO42- |
| D、Al3+、Mg2+、SO42-、CO32- |
下列说法正确的是( )
| A、已知某温度下纯水中的c(H+)=2×l0-7mol/L,据此无法求出水中c(OH-) | ||||||||||
| B、已知MgCO3的KSP=6.82×l0-6,则在含有固体MgCO3的MgCl2、Na2CO3溶液中,都有:c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2/L2 | ||||||||||
| C、常温下,Mg(OH)2能溶于氯化铵浓溶液的主要原因可能是NH4+结合OH-使沉淀溶解平衡发生移动 | ||||||||||
D、已知:
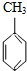 (g)+3H2(g)→ (g)+3H2(g)→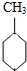 (g) 的焓变 (g) 的焓变 |