题目内容
2.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,1mol丙烷共用电子对数为10NA | |
| B. | 0.5mol甲烷和0.5mol乙酸完全燃烧消耗的O2分子数都为0.2 NA | |
| C. | 标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为$\frac{8}{22.4}$NA | |
| D. | 1mol甲醇与足量钠反应,转移电子数目为2NA |
分析 A、丙烷中含2条C-C键和8条C-H键;
B、乙酸的化学式可以写为CH4(CO2);
C、标况下辛烷为液态;
D、1mol甲醇能和1mol钠反应.
解答 解:A、丙烷中含2条C-C键和8条C-H键,故1mol丙烷中含10NA条共价键,故A正确;
B、乙酸的化学式可以写为CH4(CO2),故0.5mol甲烷和0.5mol乙酸的耗氧量相当于1mol甲烷的耗氧量,即共消耗2mol氧气即2NA个氧气分子,故B错误;
C、标况下辛烷为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故C错误;
D、1mol甲醇能和1mol钠反应,钠反应后变为+1价,故转移NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列说法正确的是( )
| A. | 氯气溶于水的离子方程式:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,若溶液变成蓝色,则氧化性:Cl2>I2 | |
| C. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| D. | 漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
17.下列食物中富含维生素的是( )
| A. | 牛奶 | B. | 白糖 | C. | 青菜 | D. | 植物油 |
11.关于化学键的下列叙述中,不正确的是( )
| A. | 离子化合物可能含共价键 | B. | 共价化合物可能含离子键 | ||
| C. | 离子化合物中一定含离子键 | D. | 共价化合物中不含离子键 |
12.香兰素是重要的香料之一,它可由丁香酚合成,如图所示,有关两种化合物的说法正确的是( )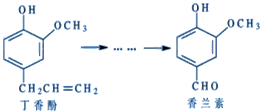

| A. | 常温下,1 mol丁香酚只能与1 mol Br2反应 | |
| B. | 丁香酚不能与FeCl3溶液发生显色反应 | |
| C. | 1 mol香兰素最多能与3 mol氢气发生加成反应 | |
| D. | 香兰素分子中至少有12个原子共平面 |
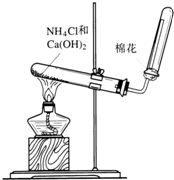 如图是实验室制取氨气的装置图.请回答:
如图是实验室制取氨气的装置图.请回答: