题目内容
12.下列说法正确的是( )| A. | 氯气溶于水的离子方程式:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,若溶液变成蓝色,则氧化性:Cl2>I2 | |
| C. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| D. | 漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
分析 A、次氯酸是弱电解质,用化学式;
B、氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色,同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
C、氯水中含HClO,具有漂白性;
D、漂白粉在空气中久置变质,是因为次氯酸钙吸收二氧化碳反应生成碳酸钙和次氯酸,次氯酸见光分解使漂白粉变质.
解答 解:A、次氯酸是弱电解质,氯气溶于水的离子方程式:Cl2+H2O═H++Cl-+HClO,故A错误;
B、氯气具有强氧化性,能氧化碘离子生成碘,碘遇淀粉试液变蓝色,同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,该反应中氯气是氧化剂、碘是氧化产物,则氧化性:Cl2>I2,故B正确;
C、氯水中含HClO,具有漂白性,不能利用pH试纸测pH,应选pH计测定,故C错误;
D、漂白粉在空气中久置变质,是因为次氯酸钙吸收二氧化碳反应生成碳酸钙和次氯酸,次氯酸见光分解使漂白粉变质,解释不正确,故D错误;
故选B.
点评 本题考查了物质性质和应用的分析判断,注意氧化还原反应的理解应用,次氯酸变质是指次氯酸分解失效,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列实验装置或操作与粒子的大小无直接关系的是( )
| A. | 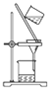 过滤 | B. | 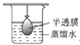 渗析 | C. | 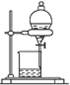 分液 | D. | 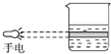 丁达尔效应 |
3.下列变化过程不包含化学变化的是( )
| A. | 煤的干馏 | B. | 煤的气化 | C. | 煤的液化 | D. | 石油分馏 |
20.合成氨的反应为:3H2+N2?2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol•L-1•s-1),则下列关系正确的是( )
| A. | v(H2)=v(N2)=v(NH3) | B. | 3 v(H2)=v(N2) | C. | 2 v(N2)=v(NH3) | D. | v(NH3)=3/2v(H2) |
7.甲醇(CH3OH)燃料电池是一种效率高,污染小的电池,该电池在碱性条件下工作时,有关说法错误的是( )
| A. | 甲醇发生氧化反应 | |
| B. | O2在电极上得电子,被还原 | |
| C. | 电池工作时,甲醇电极反应式:CH3OH-6e-+H2O=CO2↑+6H+ | |
| D. | 该电池的甲醇燃料并没有储存在电池内部 |
17.有关颜色变化与氧化还原反应有关的是( )
| A. | 苯使溴水褪色 | |
| B. | 长时间放置的KI溶液变棕色 | |
| C. | 将Na2CO3溶液点在红色石蕊试纸上,试纸变蓝 | |
| D. | 向KSCN与FeCl3的混合溶液中加入FeCl3晶体,溶液颜色加深 |
5.把铁片放入下列溶液中,铁片溶解,并有气体放出的是( )
| A. | 稀硫酸 | B. | CuSO4溶液 | C. | Fe2(SO4)3溶液 | D. | AgNO3溶液 |
2.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,1mol丙烷共用电子对数为10NA | |
| B. | 0.5mol甲烷和0.5mol乙酸完全燃烧消耗的O2分子数都为0.2 NA | |
| C. | 标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为$\frac{8}{22.4}$NA | |
| D. | 1mol甲醇与足量钠反应,转移电子数目为2NA |