题目内容
室温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴加甲基橙试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- |
| B、水电离出的c(H+)=10-12mol/L的溶液中:K+、Na+、SO4 2-、AlO2- |
| C、能与铝反应生成氢气的溶液中:Mg2+、Na+、Cl-、NO3- |
| D、滴入KSCN显血红色的溶液中:NH4+、Mg2+、SO42-、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:A.滴加甲基橙试剂显红色的溶液呈酸性;
B.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
C.能与铝反应生成氢气的溶液可能为非氧化性酸或强碱性溶液;
D.滴入KSCN显血红色的溶液含有Fe3+.
B.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性;
C.能与铝反应生成氢气的溶液可能为非氧化性酸或强碱性溶液;
D.滴入KSCN显血红色的溶液含有Fe3+.
解答:
解:A.滴加甲基橙试剂显红色的溶液呈酸性,酸性条件下,Fe2+与NO3-发生氧化还原反应而不能大量共存,故A错误;
B.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下AlO2-不能大量共存,故B错误;
C.能与铝反应生成氢气的溶液可能为非氧化性酸或强碱性溶液,碱性条件下Mg2+不能大量共存,故C错误;
D.滴入KSCN显血红色的溶液含有Fe3+,离子之间不发生任何反应,可大量共存,故D正确.
故选D
B.水电离出的c(H+)=10-12mol/L的溶液,水的电离受到抑制,溶液可能呈酸性,也可能呈碱性,酸性条件下AlO2-不能大量共存,故B错误;
C.能与铝反应生成氢气的溶液可能为非氧化性酸或强碱性溶液,碱性条件下Mg2+不能大量共存,故C错误;
D.滴入KSCN显血红色的溶液含有Fe3+,离子之间不发生任何反应,可大量共存,故D正确.
故选D
点评:本题考查离子共存,为高考常见题型,侧重于学生的分析能力和综合运用化学知识的考查,把握离子的性质以及题目隐含信息,答题时注意审题,难度不大.

练习册系列答案
相关题目
向三份等体积、等浓度的KOH溶液中分别滴加等pH的硫酸、盐酸和醋酸三种酸溶液,将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是( )
| A、V3>V2>V1 |
| B、V3=V2=V1 |
| C、V3>V2=V1 |
| D、V1=V2>V3 |
下列离子方程式中错误的是( )
| A、碳酸镁与H2SO4反应:MgCO3+2H+=Mg2++H2O+CO2↑ |
| B、向硝酸银溶液中加盐酸:Ag++Cl-=AgCl↓ |
| C、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| D、澄清石灰水与盐酸的反应:H++OH-=H2O |
水的电离过程为H2O?H++OH-,在25℃时,水的离子积:KW=1×10-14,在35℃时,水的离子积:KW(35℃)=2.1×10-14,则下列叙述正确的是( )
| A、c(H+)随着温度的升高而降低 |
| B、35℃时,c(H+)<c(OH-) |
| C、35℃时的水比25℃时的水电离程度小 |
| D、水的电离是吸热的 |
下列有机物的系统命名中正确的是( )
| A、CH3CH(C2H5)CH3 2-乙基丙烷 |
| B、CH3CH2CH2CH2OH 1-丁醇 |
C、 间二甲苯 间二甲苯 |
D、 2-甲基-2-丙烯 2-甲基-2-丙烯 |
下列物质属于电解质的是( )
| A、CO2 |
| B、浓硫酸 |
| C、蔗糖 |
| D、NaCl |
 某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E表示活化能),下列叙述正确的是( )| A、逆反应的活化能大于正反应的活化能 |
| B、该反应为放热反应 |
| C、催化剂能改变反应的焓变 |
| D、催化剂能降低反应的活化能 |
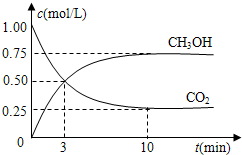 在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.
在体积为1L的密闭容器中(体积不变),充入1mol CO2和3mol H2,一定条件下发生如下反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CO2和CH3OH(g)的浓度随时间变化如图.