题目内容
11.下列事实不能说明CH3COOH位弱酸的是( )| A. | 测得0.10mol/LCH3COOH溶液中存在较多的CH3COOH分子 | |
| B. | 比较等浓度等体积的盐酸、CH3COOH溶液与足量Zn反应生成H2的体积 | |
| C. | 比较等浓度等体积的盐酸、CH3COOH溶液与等量NaOH溶液反应后放出的热量 | |
| D. | 0.10mol/LNH4Cl呈酸性,0.1mol/LCH3COONH4溶液呈中性 |
分析 部分电离的电解质是弱电解质,要说明CH3COOH是弱酸,只要证明CH3COOH部分电离即可,可以根据一定浓度溶液pH、其钠盐溶液酸碱性等判断.
解答 解:A.测得0.10mol/LCH3COOH溶液中存在较多的CH3COOH分子,说明醋酸部分电离,所以能说明醋酸是弱酸,故A不选;
B.等浓度等体积的盐酸、CH3COOH溶液与足量Zn反应生成H2的体积相同,与酸性强弱无关,则不能证明醋酸是弱酸,故B选;
C.弱酸电离过程会吸热,所以等浓度等体积的盐酸、CH3COOH溶液与等量NaOH溶液反应后放出的热量,醋酸少,说明醋酸是弱酸,故C不选;
D.0.10mol/LNH4Cl呈酸性,0.1mol/LCH3COONH4溶液呈中性,说明醋酸根离子的水解程度与铵根离子的水解程度相同,即醋酸为弱酸,故D不选;
故选B.
点评 本题考查强弱电解质的判断,明确强弱电解质的根本区别是解本题关键,题目难度不大,注意把握弱电解质在溶液中部分电离的特点,侧重于考查的分析能力和应用能力.

练习册系列答案
相关题目
4.下列能级中轨道数最多的是( )
| A. | f能级 | B. | d能级 | C. | s能级 | D. | p级 |
3.常温下,下列各组离子能在指定溶液中大量共存的是( )
| A. | 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-12mol/L,的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | PH=0的溶液中:Al3+、Ag(NH3)2+、I-、SO42- | |
| D. | 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3- |
19.下列物质的水溶液因水解呈碱性的是( )
| A. | HCl | B. | NaOH | C. | CH3COONa | D. | Na2SO4 |
6.下列反应的离子方程式正确的是( )
| A. | 制作印刷电路板:Fe3++Cu═Cu2++Fe2+ | |
| B. | 等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | Ca(OH)2溶液与足量Ca(HCO3)2溶液反应:Ca2++2HCO3-+2OH-═2CaCO3↓+2H2O+CO32- | |
| D. | 新制饱和氯水中加入石灰石可提高溶液中HClO浓度:CaCO3+2Cl2+H2O═Ca2++2Cl-+CO2↑+2H2O |
16.某工业废水中仅含下表离子中的5种:
某同学欲探究废水的组成,进行了如下实验:
Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
Ⅱ.向Ⅰ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
下列推断不正确的是( )
| 阳离子 | K+、Cu2+、Fe3+、Ca2+、Fe2+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
Ⅰ.取废水少许加入足量盐酸,无白色沉淀析出,但生成能使澄清石灰水变浑浊的无色无味气体
Ⅱ.向Ⅰ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
下列推断不正确的是( )
| A. | 溶液中一定含有的离子是K+、Cl-、CO32-、NO3-、SO42- | |
| B. | Ⅰ中加入盐酸生成无色气体的离子方程式是CO32-+2H+═CO2↑+H2O | |
| C. | 原溶液中的K+、Cl-、NO3-存在与否无法确定 | |
| D. | Ⅱ中产生白色沉淀的离子方程式是Ba2++SO42-═BaSO4↓ |
3.下列关于有机化合物的叙述正确的是( )
| A. | 氟利昂-12的结构式为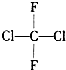 ,该分子是平面型分子 ,该分子是平面型分子 | |
| B. | 苯与液溴混合后撤入铁粉发生了加成反应 | |
| C. | 分子式为C4H9Cl的同分异构体共有4种 | |
| D. | 1mol苹果酸(HOOCCHOHCH2COOH)可与3molNaHCO3发生反应 |
20.薄荷醇的结构简式如图,下列说法正确的是( )
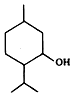

| A. | 薄荷醇属于芳香烃的含氧衍生物 | |
| B. | 薄荷醇分子式为C10H20O,它是环己醇的同系物 | |
| C. | 薄荷醇环上的一氯取代物只有三种 | |
| D. | 在一定条件下,薄荷醇能与氢气、溴水反应 |
2.某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等):
(1)该盐酸的物质的量浓度为3.0mol/L
(2)第III组实验后,剰余NaHCO3的物质的量为0.075mol.
| 实验序号 | I | II | III |
| 盐酸体积(mL) | 50.0 | 50.0 | 50.0 |
| 样品质量/g | 9.2 | 15.7 | 27.6 |
| CO2体积/L (标准状况) | 2.24 | 3.36 | 3.36 |
(2)第III组实验后,剰余NaHCO3的物质的量为0.075mol.