题目内容
3.有八种物质:①乙酸、②苯、③聚乙烯、④苯酚、⑤2-丁炔、⑥甲醛、⑦邻-二甲苯、⑧环己烯,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )| A. | ④⑤⑥⑧ | B. | ④⑤⑦⑧ | C. | ③④⑤⑧ | D. | ③④⑤⑦⑧ |
分析 既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,则有机物含碳碳双键、碳碳三键、-CHO、酚-OH等,以此来解答.
解答 解:①乙酸与溴水、高锰酸钾均不反应,故不选;
②苯与溴水、高锰酸钾均不反应,故不选;
③聚乙烯不含碳碳双键,与溴水、高锰酸钾均不反应,故不选;
④苯酚含酚-OH,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故选;
⑤2-丁炔含碳碳三键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故选;
⑥甲醛含-CHO,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故选;
⑦邻-二甲苯与溴水不反应,故不选;
⑧环己烯中含碳碳双键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故选;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质,题目难度不大.

练习册系列答案
相关题目
13.下列说法正确的是( )
①极性分子一定含有极性键,非极性分子一定含有非极性键
②极性分子中一定不含有非极性键,非极性分子中可能含有极性键
③N2O和CO2是互为等电子体,因此每个分子均含有2个π 键,且中心原子均为sp杂化
④丙酮的沸点为57℃高于丁烷的沸点为-0.5℃是由于丙酮分子间有氢键
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低与氢键有关.
①极性分子一定含有极性键,非极性分子一定含有非极性键
②极性分子中一定不含有非极性键,非极性分子中可能含有极性键
③N2O和CO2是互为等电子体,因此每个分子均含有2个π 键,且中心原子均为sp杂化
④丙酮的沸点为57℃高于丁烷的沸点为-0.5℃是由于丙酮分子间有氢键
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低与氢键有关.
| A. | ③⑤ | B. | ②④⑤ | C. | ②③④⑤ | D. | ①②③④⑤ |
14.下列各组物质的晶体中,化学键类型相同、晶体类型也相同的是( )
| A. | 金刚石和SiO2 | B. | CO2和SiO2 | C. | NaCl和 HCl | D. | 钠和KCl |
18.A、B属于短周期元素,A的阳离子与B的阴离子具有相同的电子层结构.以下关于A、B的比较中,不正确的是( )
| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层电子数:B>A | D. | 元素所在的周期数:A>B |
8.下列判断正确的是( )
①阴离子都只有还原性
②NO2溶于水时发生氧化还原反应
③1mol Cl2参加反应转移电子数一定为2NA
④BaSO3和H2O2的反应为氧化还原反应.
①阴离子都只有还原性
②NO2溶于水时发生氧化还原反应
③1mol Cl2参加反应转移电子数一定为2NA
④BaSO3和H2O2的反应为氧化还原反应.
| A. | ②④ | B. | ②③ | C. | ③④ | D. | ①④ |
12.X是某元素的一种同位素,该原子的质量数为A,中子数为N,它的气态氢化物为XH3,则它与18O形成的最高价气态氧化物ag中含有质子的物质的量为( )
| A. | $\frac{a(A-N+3)}{A+3}$mol | B. | $\frac{a(A-N+8)}{A+16}$mol | ||
| C. | $\frac{a(2A-2N+40)}{2A+90}$mol | D. | $\frac{2A-2N+24}{2A+54}$mol |
19.某一元醛发生银镜反应可得21.6g银,将等量的醛完全燃烧,生成3.6g H2O,此醛可能是( )
| A. | 乙醛 | B. | 丙醛 | C. | 丁醛 | D. | 戊醛 |
 已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答:
已知前四周期六种元素A、B、C、D、E、F的核电荷数依次增大.B原子的p轨道半充满,其氢化物沸点是同族元素中最低的,D原子得到一个电子后3p轨道全充满,A与C能形成AC型离子化合物,其中的阴、阳离子相差一个电子层.E4+离子和氩原子的核外电子排布相同,F元素含量决定了人体内血红蛋白携氧能力的大小.请回答: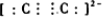 ,其中α键和π键数目之比为1:2.
,其中α键和π键数目之比为1:2.