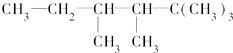题目内容
15.已知碳元素能形成多种金属碳化物,如碳化钙,俗称为电石.(1)电石(CaC2)是用CaO与焦炭在电炉中加强热反应生成的,写出此反应的化学方程式CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO,CaC2中含有化学键的类型为离子键和非极性共价键,C22-与N2互为等电子体,C22-的电子式可表示为
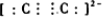 ,其中α键和π键数目之比为1:2.
,其中α键和π键数目之比为1:2.(2)已知MgO、CaO的熔点分别为2852℃、2614℃,分析熔点差异的原因是氧化镁的晶格能大于氧化钙.
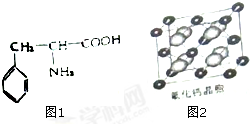
(3)苯丙氨酸是一种重要的氨基酸,其结构如图1所示,分子中第一电离能最大的原子价电子排布式是s2sp3,其中碳原子的杂化方式有sp2、sp3.
(4)已知CaF2晶体(如图2,Ca2+处于面心)的密度为ρg/cm3,NA为阿伏加德常数,相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量(M)可以表示为$\frac{{a}^{3}ρ{N}_{A}}{4}$g/mol.
分析 (1)CaO与焦炭在电炉中加强热反应生成的,化学反应方程式为:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO;CaC2中含有化学键的类型为离子键和非极性共价键;C22-含有C≡C键,电子式为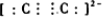 ;
;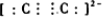 中含有1个σ和2个π;
中含有1个σ和2个π;
(2)MgO、CaO两者都是离子晶体,晶格能的大小不同,导致熔沸点的不同;
(3)苯丙氨酸是一种重要的氨基酸,其结构如图1所示,分子中第一电离能最大的原子是氮原子,价电子排布式是2s2sp3;苯环和羧基上的碳是sp2杂化,其余碳是sp3杂化;
(4)根据ρV=$\frac{M}{{N}_{A}}$计算相对分子质量.
解答 解:(1)CaO与焦炭在电炉中加强热反应生成的,化学反应方程式为:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO;CaC2中含有化学键的类型为离子键和非极性共价键;C22-含有C≡C键,电子式为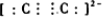 ,α键和π键数目之比为1:2,故答案为:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO;离子键和非极性共价键;
,α键和π键数目之比为1:2,故答案为:CaO+3C$\frac{\underline{\;高温\;}}{\;}$CaC2+CO;离子键和非极性共价键;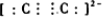 ;1:2;
;1:2;
(2)MgO、CaO两者都是离子晶体,镁离子的半径小钙离子的半径,因为氧化镁的晶格能大于氧化钙,所以MgO的熔点高于CaO的熔点,故答案为:氧化镁的晶格能大于氧化钙;
(3)苯丙氨酸是一种重要的氨基酸,其结构如图1所示,分子中第一电离能最大的原子是氮原子,价电子排布式是2s2sp3;苯环和羧基上的碳是sp2杂化,其余碳是sp3杂化,故答案为:2s2sp3;sp2、sp3;
(4)该晶胞中含有钙离子个数=$\frac{1}{8}$×8+$\frac{1}{2}$×6=4,根据一个晶胞的质量为ρV=$\frac{M}{{N}_{A}}$,Ca的摩尔质量在数值上和其相对分子质量是相等的,即M=ρVNA=$\frac{{a}^{3}ρ{N}_{A}}{4}$,故答案为:$\frac{{a}^{3}ρ{N}_{A}}{4}$.
点评 本题考查物质结构与性质,综合性强,涉及核外电子排布、分子结构与性质、晶格能、晶体结构与性质、杂化轨道、等电子体、晶胞计算等,侧重对主干知识的考查,需要学生熟练掌握基础知识,题目难度中等.

 全优点练单元计划系列答案
全优点练单元计划系列答案(1)TiCl4是生产金属钛和钛白的原料,工业上主要用TiO2氯化的方法来制取.
①有人拟用以下氯化反应来制取TiCl4:TiO2(s)+2Cl2(g)?TiCl4(l)+O2(g)△H=+151kJ/mol,你认为这一氯化反应是否可自发进行?理论根据是什么?反应不能自发进行,因为此反应中△H>0,△S<0,△G=△H-T•△S>0,故此反应不能自发进行.
②工业上通常往TiO2和Cl2反应体系中加入碳单质,在一定条件下制取TiCl4,从化学平衡的角度解释此方法能顺利制取TiCl4的原因加入的碳单质与氧气反应,减小了产物O2的浓度,使TiO2(s)+2Cl2(g)?TiCl4(l)+O2(g)平衡向正反应方向移动,使反应能够顺利进行.
(2)某化学实验小组以TiO2和足量 CCl4为原料制取TiCl4,装置图如图1:
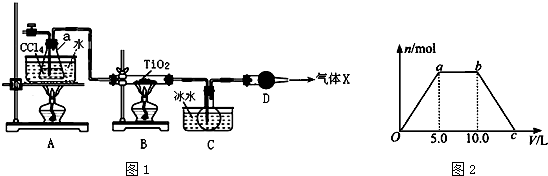
表是有关物质的性质:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76.8 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
①实验开始时先点燃A处的酒精灯,待C中烧瓶里有液滴出现时再点燃B处的酒精灯,其主要目的是先排尽系统(装置)中的空气.
②本实验中仪器a采用题给的加热方式的突出优点是受热均匀,能为反应提供稳定的CCl4蒸汽流.
③B中TiO2发生反应的化学方程式是TiO2+CCl4$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4+CO2↑.
④欲分离C装置中的TiCl4,应采用的实验操作为蒸馏(填操作名称).
⑤若将反应过程中生成的气体X(足量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图2所示,则混合稀溶液中Ba( OH)2和NaOH的物质的量之比为1:1; 从a点到b点依次发生的第一个反应的离子方程式是CO2+2OH-=CO32-+H2O.
| A. | ④⑤⑥⑧ | B. | ④⑤⑦⑧ | C. | ③④⑤⑧ | D. | ③④⑤⑦⑧ |
| A. | 冬季居民的家中用煤取暖 | B. | 城市和乡村大力开展植树造林 | ||
| C. | 工厂排放烟尘的烟囱加高 | D. | 将城市的固体废弃物运向农村倾倒 |
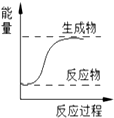
| A. | 金属钠与水的反应 | B. | 氢气燃烧 | ||
| C. | 浓硫酸的稀释 | D. | Ba(OH)2•8H2O和NH4Cl (固体)混合 |