题目内容
4.发射卫星用N2H4气体为燃料,NO2气体为氧化剂,两者反应生成N2和水蒸气,已知:N2 (g)+2O2 (g)=2NO2 (g)△H1=+67.7kJ•mol-1;
2H2 (g)+O2 (g)=2H2O(g)△H2=-484kJ•mol-1;
N2H4 (g)+O2 (g)=N2 (g)+2H2O(g)△H3=-534kJ•mol-1;
H2 (g)+F2 (g)=2HF(g)△H4=-538kJ•mol-1;
H2O(1)=H2O(g)△H5=+44.0kJ•mol-1.
①写出N2H4气体与NO2气体反应生成氮气和液态水的热化学方程式:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)△H=-1311.7kJ/mol
②写出N2H4气体与F2气体反应的热化学方程式N2H4(g)+2F2(g)=N2(g)+4HF(g)△H=-1126KJ/mol.
分析 (1)已知:①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ•mol-1;
③N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ•mol-1;
⑤H2O(l)=H2O(g)△H3=+44.0kJ•mol-1.
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)可以是反应③×2-①-⑤×4得到,由此分析解答;
(2)②2H2(g)+O2(g)=2H2O (g)△H2=-484kJ/mol;
③N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol;
④H2(g)+F2(g)=2HF(g)△H4=-538kJ/mol
依据盖斯定律④×2-②+③得到,由此分析解答.
解答 解:(1)已知:①N2(g)+2O2(g)=2NO2(g)△H1=+67.7kJ•mol-1;
③N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ•mol-1;
⑤H2O(l)=H2O(g)△H3=+44.0kJ•mol-1.
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)可以是反应③×2-①-⑤×4得到,
所以该反应的焓变=(-534kJ•mol-1)×2-67.7kJ•mol-1-(+44kJ•mol-1)×4=-1311.7kJ/mol,
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l)△H=-1311.7kJ/mol;
(2)②2H2(g)+O2(g)=2H2O (g)△H2=-484kJ/mol;
③N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=-534kJ/mol;
④H2(g)+F2(g)=2HF(g)△H4=-538kJ/mol
依据盖斯定律④×2-②+③得到热化学方程式为:N2H4(g)+2F2(g)=N2(g)+4HF(g)△H=-1126KJ/mol;
故答案为:N2H4(g)+2F2(g)=N2(g)+4HF(g)△H=-1126KJ/mol.
点评 本题考查了热化学方程式的书写方法和盖斯定律的计算应用,题目较简单.

| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 反应达到平衡时,X的转化率为50% | |
| B. | 反应可表示为X+3Y?2Z,平衡常数为1600 | |
| C. | 其他条件不变时,增大压强可使平衡常数增大 | |
| D. | 改变温度可以改变该反应的平衡常数 |
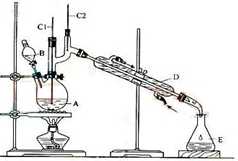 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.Na2Cr2O7H2SO4加热
发生的反应如下:
CH3CH2CH2CH2OH$\frac{\underline{\;\;\;Na_{2}Cr_{2}O_{7}\;\;\;}}{H_{2}SO_{4}加热}$ CH3CH2CH2CHO
反应物和产物的相关数据列表如表:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分.将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.4g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止液体暴沸.若加热后发现未加沸石,应采取的正确方法是冷却后补加.
(3)装置图中,D仪器的名称是滴液漏斗,B仪器的名称是直形冷凝管,冷水从下进.(填上或下)
(4)分液漏斗使用前必须进行的操作是b(填正确答案标号).
a.润湿 b.检漏 c.干燥 d.标定
(5)将正丁醛粗产品置于分液漏斗中分层时,水在下 层(填“上”或“下”)
(6)本实验中,正丁醛的产率为62.5%.
(7)反应温度应保持在90-95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(2)已知反应N2+3H2?2NH3△H=a kJ•mol-1.试根据下表中所列键能数据估算a的数值为-93.
| 化学键 | H-H | N-H | N≡N |
| 键能kJ/mol | 436 | 391 | 945 |
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应热化学方程式:2C (s,石墨)+H2(g)=C2H2(g)△H=+226.7kJ/mol.
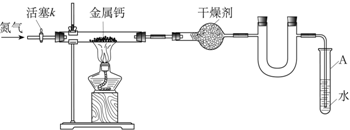
(1)按图连接好实验装置.检查装置气密性的方法是关闭活塞k,将末端导管插入试管A的水中,用酒精灯微热硬玻璃管,若导管末端有气泡冒出,撤去酒精灯冷却后,在导管内形成一段水柱,则证明装置的气密性良好.
(2)反应过程中末端导管必须插入试管A 的水中,目的是防止空气中的氧气通过末端导管进入实验装置,生成氧化钙,引入杂质
(3)制备氮化钙的操作步骤是:
①打开活塞k并通入N2;
②点燃酒精灯,进行反应;
③反应结束后
④拆除装置,取出产物.
(4)数据记录如下:
| 空硬玻璃管质量m0/g | 硬玻璃管与钙的质量m1/g | 硬玻璃管与产物的质量m2/g |
| 114.8 | 120.8 | 122.2 |
②若通入的N2中混有少量O2,如上计算得到的x3<3(填写“>”、“=”、“<”),判断依据
是:因为钙的总量不变,含有氧化钙的氮化钙总质量增大,钙与氮(不纯)元素的质量比减小,其个数比也变小,所以x值会减小.
| A. | 标准状况下,22.4 L 水蒸气含有的分子数为1NA | |
| B. | 常温常压下,32 g O2含有的原子数为2个 | |
| C. | 常温常压下,NA个CO2分子占有的体积为22.4 L | |
| D. | 体积为1L、物质的量浓度为0.5 mol/L的氯化钙溶液中,含有Cl-个数为1NA |
 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.