��Ŀ����
9����25��ʱ���ܱ�������X��Y��Z�����������ʼŨ�Ⱥ�ƽ��Ũ�����������˵��������ǣ�������| ���� | X | Y | Z |
| ��ʼŨ��/mol•L-1 | 0.1 | 0.2 | 0 |
| ƽ��Ũ��/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A�� | ��Ӧ�ﵽƽ��ʱ��X��ת����Ϊ50% | |
| B�� | ��Ӧ�ɱ�ʾΪX+3Y?2Z��ƽ�ⳣ��Ϊ1600 | |
| C�� | ������������ʱ������ѹǿ��ʹƽ�ⳣ������ | |
| D�� | �ı��¶ȿ��Ըı�÷�Ӧ��ƽ�ⳣ�� |
���� X��Y��Ũ�ȼ�С��Ϊ��Ӧ�Z��Ũ������Ϊ�����Ũ�ȱ仯��֮�ȣ�0.1-0.05������0.2-0.05������0.1-0��=1��3��2����ӦΪX+3Y?2Z��
A��ת����=$\frac{ת������}{��ʼ����}$��100%��
B��KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ����ƽ��Ũ�ȼ���K��
C��Kֻ���¶��йأ�
D��Kֻ���¶��йأ��ı��¶ȣ�Kһ���仯��
��� �⣺X��Y��Ũ�ȼ�С��Ϊ��Ӧ�Z��Ũ������Ϊ�����Ũ�ȱ仯��֮�ȣ�0.1-0.05������0.2-0.05������0.1-0��=1��3��2����ӦΪX+3Y?2Z��
A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ$\frac{0.1-0.05}{0.1}$��100%=50%����A��ȷ��
B��X+3Y?2Z��K=$\frac{0��{1}^{2}}{0.05����0.05��^{3}}$=1600����B��ȷ��
C��Kֻ���¶��йأ�������ѹǿʱƽ�ⳣ�����䣬��C����
D��Kֻ���¶��йأ��ı��¶ȿ��Ըı�÷�Ӧ��ƽ�ⳣ������D��ȷ��
��ѡC��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����Ũ�ȱ仯����Ӧ��ȷ����K�ļ��㡢K���¶ȵĹ�ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע������ƽ��Ũ�ȼ���K����Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д� �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
�����Ŀ
19����һ��չ̶�������ܱ������У�����10mol N2��30mol H2��Ϻ�����Ӧ��N2+3H2?2NH3����һ���¶��´ﵽƽ�⣬H2��ת����Ϊ20%������ͬһ�����г���NH3����ʹ��Ӧ�ﵽƽ��ʱ���ɷֵİٷֺ���������ƽ��ʱ��ͬ������ʼʱ����NH3�����ʵ����ʹﵽƽ��ʱNH3��ת�����ǣ�������
| A�� | 15mol 20% | B�� | 20mol 20% | C�� | 20mol 80% | D�� | 40mol 80% |
20���������и�װ��ͼ�������У���ȷ���ǣ�������
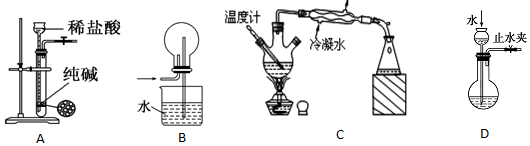

| A�� | ��ͼAװ����ȡ����CO2���� | |
| B�� | �����NH3����ͼBװ������ | |
| C�� | װ��C�ɷ���е㲻ͬ�һ��ܵ�Һ������ | |
| D�� | ͼD�ɼ��װ�õ������� |
17����Һ�����塢��Һ���ַ�ɢϵ��ʵ������ǣ�������
| A�� | �ȶ��� | B�� | ���� | ||
| C�� | �ܷ������������ | D�� | ��ɢ������С |
4����֪Cu2O�������ᷴӦ������ʽΪ��3Cu2O+14HNO3�T6Cu��NO3��2+2NO��+7H2O��������NO�����Ϊ 0.448L������£���������˵����ȷ���ǣ�������
| A�� | ��������Cu2OΪ1.44 g | |
| B�� | ��������������Ϊ0.14 mol | |
| C�� | ������0.5 moI/L����140 mL��Cu2O��Ӧ | |
| D�� | ת�Ƶĵ�������Ϊ0.06 NA |
14������˵������ȷ���ǣ�������
| A�� | 1molC������12 g•mol-1 | |
| B�� | 22.4L H2�����ʵ�����1mol | |
| C�� | ��60gNaOH����1Lˮ�У�������Һ��NaOH�����ʵ���Ũ����1.5mol•L-1 | |
| D�� | NaCl��Ħ��������58.5 g•mol-1 |
6����һ���¶��£�����ͭ������������д�������ƽ�⣺Cu2+��aq��+SO42-��aq��+xH2O��l��?CuSO4•xH2O��s����������Һ�м�������ˮ����ͭ��ĩ������˵������ȷ���ǣ�������
| A�� | ��Һ��Cu2+Ũ������ | B�� | ��Һ��Cu2+��Ŀ���� | ||
| C�� | ����Һ��pH��С | D�� | ��Һ����ɫ��dz |
3���ȱ�����Ҫ���л�������Ʒ����Ⱦ�ϡ�ҽҩ���л��ϳɵ��м��壬��ҵ�ϳ��á���϶������ȡ����Ӧԭ����ʵ��װ��ͼ������װ�ö�����ȥ�����£�
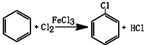
��֪���ȱ�Ϊ��ɫҺ�壬�е�132.2�森
�ش��������⣺
��1��A��Ӧ��������ʵ���ҷ���ȡ�������пղ�����B��������ƽ����ѹ������������ˮӦ��a���a����b���� ��ͨ�룮
��2���Ѹ��������ͨ��װ�и��ﱽ�ķ�Ӧ��C�У������൱�ڱ���1%����м��������������ά�ַ�Ӧ�¶���40��60��Ϊ�ˣ��¶ȹ������ɶ��ȱ���
�ٶ�C���ȵķ�����c������ţ�
a���ƾ��Ƽ��� b����ԡ���� c��ˮԡ����
��D���ڵ�����ɷ���HCl����������������
��3��C��Ӧ����Ӧ��ɺ�ҵ��Ҫ����ˮϴ����ϴ��ʳ�θ����������ϴ֮ǰҪˮϴ��Ŀ����ϴȥ�������ͬʱ���ټ����������Լ�ɱ���д����10%�������Ƽ�ϴʱ���ܷ����Ļ�ѧ��Ӧ����ʽ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O����д�������ɣ�
��4������װ��ͼ��A��C��Ӧ��֮�䣬��Ҫ����һ��U�ιܣ������������������������Ȼ��ƣ�
��5����ҵ�����б�����ʧ������£�
��lt�����Ƶó�ƷΪ$\frac{��1-0.0892����112.5}{78}$t��ֻҪ����ʽ����

��֪���ȱ�Ϊ��ɫҺ�壬�е�132.2�森
�ش��������⣺
��1��A��Ӧ��������ʵ���ҷ���ȡ�������пղ�����B��������ƽ����ѹ������������ˮӦ��a���a����b���� ��ͨ�룮
��2���Ѹ��������ͨ��װ�и��ﱽ�ķ�Ӧ��C�У������൱�ڱ���1%����м��������������ά�ַ�Ӧ�¶���40��60��Ϊ�ˣ��¶ȹ������ɶ��ȱ���
�ٶ�C���ȵķ�����c������ţ�
a���ƾ��Ƽ��� b����ԡ���� c��ˮԡ����
��D���ڵ�����ɷ���HCl����������������
��3��C��Ӧ����Ӧ��ɺ�ҵ��Ҫ����ˮϴ����ϴ��ʳ�θ����������ϴ֮ǰҪˮϴ��Ŀ����ϴȥ�������ͬʱ���ټ����������Լ�ɱ���д����10%�������Ƽ�ϴʱ���ܷ����Ļ�ѧ��Ӧ����ʽ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O����д�������ɣ�
��4������װ��ͼ��A��C��Ӧ��֮�䣬��Ҫ����һ��U�ιܣ������������������������Ȼ��ƣ�
��5����ҵ�����б�����ʧ������£�
| ��Ŀ | ���ȱ� | β�� | ��ȷ������ | ��ʧ���� |
| ����ʧ����kg/t�� | 13 | 24.9 | 51.3 | 89.2 |