题目内容
9.设阿伏加德罗常数为NA,则下列说法正确的是( )| A. | 乙烯、丙烯、丁烯的混合气体共14g,其含有的原子数为3NA | |
| B. | 15g甲基(-CH3)所含有的电子数为10NA | |
| C. | 1.8g重水(D2O)含质子数为NA | |
| D. | 标准状况下,11.2L二氯甲烷所含分子数为0.5NA |
分析 A.乙烯、丙烯(C3H6)、丁烯(C4H8)的最简式相同,混合物的最简式为CH2,据此计算;
B.1个甲基含有9个电子;
C.重水的摩尔质量为20g/mol,1.8g重水的物质的量为0.09mol,重水中含有10个质子;
D.气体摩尔解题使用对象为气体.
解答 解:A.混合物的最简式为CH2,使用含有的原子数为$\frac{14g}{14g/mol}$×3×NAmol-=3NA,故A正确;
B.15g甲基(-CH3)物质的量为$\frac{15g}{15g/mol}$=1mol,含有电子数9NA,故B错误;
C.1.8g重水的物质的量为0.09mol,0.09mol重水中含有0.9mol质子,含有的质子数为0.9NA,故C错误;
D.标况下,二氯甲烷为液体,不能使用气体摩尔体积,故D错误;
故选:A.
点评 本题考查阿伏加德罗常数,题目难度不大,掌握公式的使用和物质的结构、状态是解题关键,注意甲基、重水分子中含有质子数数目.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
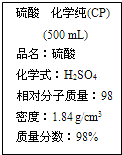

| A. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L | |
| B. | 1 mol Mg与足量该硫酸反应产生2 g氢气 | |
| C. | 配制250 mL 1.0 mol/L的稀硫酸需取该硫酸约13.6mL | |
| D. | 该硫酸溶液可作H2S的干燥剂 |
17.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| B. | 0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA | |
| C. | 由2H和18O所组成的水11g,其中所含的中子数为5NA | |
| D. | 1L0.1mol•L-1Na2CO3溶液中含有的阴离子数为0.1NA |
1.下列离子方程式不正确的是( )
| A. | 苯酚与纯碱溶液混合反应的离子方程式:2C6H5OH+CO32-→CO2↑+H2O+2C6H5O- | |
| B. | 苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| C. | 醋酸溶液与新制氢氧化铜:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| D. | 乙酸与碳酸钠溶液反应:2 CH3COOH+CO32-→2CH3COO-+CO2↑+H2O |
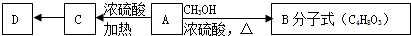

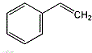 .
.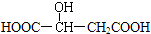 .
.