题目内容
19.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )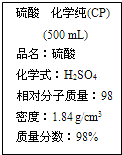
| A. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L | |
| B. | 1 mol Mg与足量该硫酸反应产生2 g氢气 | |
| C. | 配制250 mL 1.0 mol/L的稀硫酸需取该硫酸约13.6mL | |
| D. | 该硫酸溶液可作H2S的干燥剂 |
分析 A.浓硫酸浓度越大其密度越大,硫酸密度大于水密度,等质量硫酸和水,水的体积大于硫酸体积;
B.Mg和浓硫酸反应生成二氧化硫;
C.根据c=$\frac{1000ρω}{M}$计算出该硫酸的浓度,溶液配制过程中溶质的物质的量不变,据此计算出需要该浓硫酸的体积;
D.浓硫酸具有强氧化性,能够氧化硫化氢.
解答 解:A.浓硫酸浓度越大其密度越大,硫酸密度大于水密度,等质量硫酸和水,水的体积大于硫酸体积,所以二者混合后溶液体积大于浓硫酸的二倍,则其物质的量浓度小于原来的$\frac{1}{2}$,即小于9.2mol/L,故A错误;
B.Mg和浓硫酸反应生成二氧化硫,稀硫酸和锌反应生成氢气,故B错误;
C.溶液稀释前后溶质的物质的量不变,该浓硫酸浓度为:$\frac{1000×1.84×98%}{98}$=18.4mol/L,配制250 mL 1.0 mol/L的稀硫酸需取该硫酸体积为:$\frac{1.0mol/L×0.25L}{18.4mol/L}$=0.0136L=13.6mL,故C正确;
D.H2S具有较强还原性,浓硫酸能够氧化H2S,不能用浓硫酸干燥H2S,故D错误;
故选C.
点评 本题考查物质的量浓度的有关计算,题目难度不大,明确物质的性质、溶液稀释特点等知识点即可解答,易错选项是A,浓硫酸浓度越大其密度越大,氨水浓度越大其密度越小,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
10.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| B. | 凡含有食品添加剂的食物对人体健康均有害,不可食用 | |
| C. | 为了防止缺碘而导致大脖子病,故在食盐中加入KIO3 | |
| D. | 钠钾合金可以作为原子反应堆的导热剂 |
7.一定条件下,在容积为5L密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g),半分钟后测得生成0.04molSO3.在这段时间内O2的化学反应速率为( )
| A. | 0.004(mol•L-1•min-1) | B. | 0.008(mol•L-1•min-1) | ||
| C. | 0.016(mol•L-1•min-1) | D. | 0.032(mol•L-1•min-1) |
4.A、B两种有机物组成的混合物,当混合物质量相等时,无论A、B以何种比例混合,完全燃烧产生二氧化碳的量均相等,符合这一组合的条件有:①同分异构体;②同系物;③具有相同的最简式;④含碳的质量分数相同,其中正确的是( )
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
11.碱性镍锌(NiZn)电池是一种可以替代镍氢电池的新型电池,其总反应为:2NiOOH+2H2O+Zn$?_{充电}^{放电}$2Ni(OH)2+Zn(OH)2.则下列说法中错误的是( )
| A. | 电池工作时,OH-向负极移动 | |
| B. | 放电时负极反应式:Zn-2e-+2OH-═Zn(OH)2 | |
| C. | 充电时,与外电源正极相连的电极上电极反应式为Ni(OH)2-e-+OH-═NiOOH+H2O | |
| D. | 该电池电解1L 0.3 mol/LAgNO3溶液,若产生1.12L气体(标准状况),溶液pH变为2 |
8.苯乙酸的同分异构体中属于芳香酯类的有( )种.
| A. | 6 | B. | 5 | C. | 4 | D. | 7 |
9.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 乙烯、丙烯、丁烯的混合气体共14g,其含有的原子数为3NA | |
| B. | 15g甲基(-CH3)所含有的电子数为10NA | |
| C. | 1.8g重水(D2O)含质子数为NA | |
| D. | 标准状况下,11.2L二氯甲烷所含分子数为0.5NA |
 ②N2
②N2 .
.