题目内容
15.中国计量科学研究所研制的NIM5铯原子喷泉钟,2000万年不差一秒,日前成为国际计量局认可的基准钟之一,参与国际标准时间修正.关于Cs元素,下列说法错误的是( )| A. | 137Cs和133Cs互为同位素 | B. | 单质Cs与水反应非常缓慢 | ||
| C. | 137Cs比133Cs比多个中子 | D. | 137Cs最外层只有1个电子 |
分析 A.质子数相同,中子数不同,互为同位素;
B.Cs在第IA族,活泼性比钠强;
C.根据质量数=质子数+中子数计算;
D.第IA族元素原子的最外层电子数为1.
解答 解:A.137Cs和133Cs质子数相同,中子数不同,互为同位素,故A正确;
B.Cs在第IA族,活泼性比钠强,所以Cs与水反应非常剧烈,故B错误;
C.137Cs与133Cs质子数相同,137Cs比133Cs多4个中子,故C正确;
D.137Cs属于第IA族元素,第IA族元素原子的最外层电子数为1,故D正确;
故选B.
点评 本题考查原子结构和性质,题目涉及核内质子数、质量数、质子数、中子数的关系以及同主族元素的性质,题目难度不大.

练习册系列答案
相关题目
6.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | 漂白粉溶液中通入足量二氧化硫气体:ClO-+SO2+H2O═HClO+HSO${\;}_{3}^{-}$ | |
| C. | NaHCO3溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ |
3.下列能用离子方程式“H++OH-=H2O”表示的化学反应是( )
| A. | NaOH+HCl═NaCl+H2O | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | 2KOH+MgCl2═Mg(OH)2↓+2KCl | D. | Zn+H2SO4═ZnSO4+H2↑ |
10.向一定量的Cu、Fe2O3的混合物中加入100mL 1mol•L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含
Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A. | 0.8g | B. | 1.6g | C. | 2.4g | D. | 3.2g |
5.锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3•H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O.请回答下列问题:
(1)上述方程式中涉及到的N、O元素电负性由小到大的顺序是N<O.
(2)基态S的价电子排布式为3s23p4.与Cu同周期且最外层电子数相等的元素还有K、Cr(填元素符号).
(3)PO43-的空间构型是正四面体,其中P原子的杂化方式为sp3.
(4)在硫酸铜溶液中加入过量KCN溶液,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键数目为2NA.
(5)铜晶体为面心立方最密集堆积,铜的原子半径为127.8pm,列式计算晶体铜的密度9.0g/cm3.
(6)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系.
由此可得出的判断含氧酸强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.亚磷酸(H3PO3)也是中强酸,它的结构式为 .亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O.
.亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O.
(1)上述方程式中涉及到的N、O元素电负性由小到大的顺序是N<O.
(2)基态S的价电子排布式为3s23p4.与Cu同周期且最外层电子数相等的元素还有K、Cr(填元素符号).
(3)PO43-的空间构型是正四面体,其中P原子的杂化方式为sp3.
(4)在硫酸铜溶液中加入过量KCN溶液,生成配合物[Cu(CN)4]2-,则1molCN-中含有的π键数目为2NA.
(5)铜晶体为面心立方最密集堆积,铜的原子半径为127.8pm,列式计算晶体铜的密度9.0g/cm3.
(6)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系.
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH | 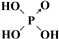 | 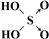 | 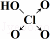 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O.
.亚磷酸与过量的氢氧化钠溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O. 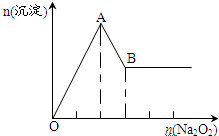 有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验
有一透明溶液,可能含有较大量的NH4+、Fe3+、Na+、SO42-、CO32-、H+、Mg2+、Al3+、Cu2+中的某一种或几种,取此溶液做下列试验