题目内容
8.等物质的量浓度的下列溶液中,导电力最强的是( )| A. | 氢氧化钠 | B. | 醋酸 | C. | 氨水 | D. | 酒精溶液 |
分析 电解质溶液导电性与离子浓度成正比,与电荷成正比,离子浓度越大其导电性越强,据此分析解答.
解答 解:电解质溶液导电性与离子浓度成正比,与电荷成正比,相同浓度的这几种溶液,醋酸和一水合氨都是弱电解质、乙醇是非电解质,NaOH是强电解质,所以这几种溶液中离子浓度最大的是氢氧化钠,则导电性最强的是NaOH,故选A.
点评 本题考查电解质溶液导电性强弱判断,为高频考点,明确电解质溶液导电性强弱影响因素是解本题关键,电解质溶液导电性与离子浓度、电荷有关,与电解质强弱、电解质溶液酸碱性无关,为易错题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其结构简式为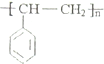 .根据所学知识,可以判断( )
.根据所学知识,可以判断( )
 .根据所学知识,可以判断( )
.根据所学知识,可以判断( )| A. | 聚苯乙烯能使溴水褪色 | |
| B. | 聚苯乙烯是一种天然高分子化合物 | |
| C. | 聚苯乙烯可由苯乙烯通过化合反应制得 | |
| D. | 聚苯乙烯单体的分子式为C8H8 |
3.下列关于氯气的叙述正确的是( )
| A. | 氢气在氯气中燃烧产生苍白色火焰 | |
| B. | 铁丝在氯气中燃烧生成FeCl2 | |
| C. | 氯气的水溶液用于漂白,是利用氯气的强氧化性 | |
| D. | 当有大量氯气逸到空气中时,可用浸有NaOH溶液的毛巾捂住鼻子 |
20.有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是( )
| A. | 氧化剂与还原剂的物质的量之比为1:8 | |
| B. | 该过程说明Fe(NO3)2溶液不宜加酸酸化 | |
| C. | 若有1 mol NO3-发生氧化反应,则转移8 mol e- | |
| D. | Fe3+的氧化性比HNO3弱 |
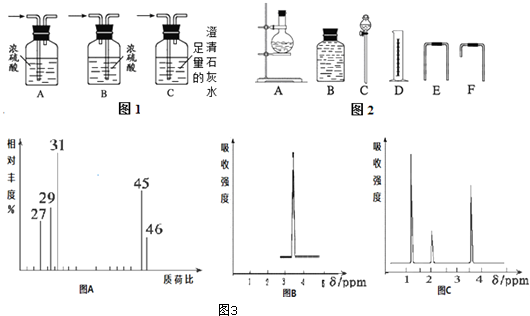
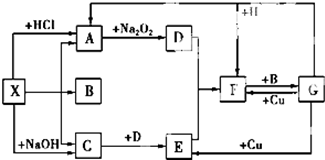 如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1molX分解得到A、B、C各1mol.试回答下列各题:
如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1molX分解得到A、B、C各1mol.试回答下列各题:
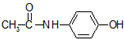 )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等.M的一种合成路线如下:
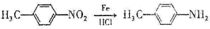 .
. ;
; ;
; ;
; .
.