题目内容
19.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 某澄清透明溶液中:K+、Cu2+、NO3-、Cl- | |
| B. | 含0.1mol•L-1 Fe3+的溶液中:Na+、Mg2+、SO42-、Cl-、SCN- | |
| C. | 含0.1mol•L-1 CO32-的溶液中:OH-、Cl-、NH4+、Na+、H+ | |
| D. | 加入铝粉产生H2的溶液中:Al3+、Na+、SO42-、NO3- |
分析 A.四种离子之间不反应,为澄清透明溶液;
B.铁离子与硫氰根离子反应;
C.碳酸根离子、氢氧根离子都与氢离子反应;
D.加入铝粉产生H2的溶液呈酸性或强碱性,铝离子与氢氧根离子反应,硝酸根离子在酸性条件下与铝反应不会生成氢气.
解答 解:A.K+、Cu2+、NO3-、Cl-之间不发生反应,能够大量共存,且为澄清透明的溶液,故A正确;
B.Fe3+和SCN-之间发生络合反应,在溶液中不能大量共存,故B错误;
C.CO32-、OH-都与H+发生反应,在溶液中不能大量共存,故C错误;
D.加入铝粉产生H2的溶液中存在大量氢离子或氢氧根离子,Al3+与氢氧根离子反应,NO3-在酸性条件下具有强氧化性,与铝反应不会生成氢气,故D错误;
故选A.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
10.下列事实中,不能用勒夏特列原理解释的是( )
| A. | 合成NH3反应,为提高NH3的产率,理论上应采取相对较低的温度 | |
| B. | 实验室中常用排饱和食盐水的方式收集氯气 | |
| C. | 对于CO(g)+NO2(g)?CO2(g)+NO(g)的平衡体系,增大压强可使颜色变深 | |
| D. | 对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
7.下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
| A. | 在标准状况下,22.4L水所含分子数目为NA | |
| B. | 1mol•L-1 K2SO4溶液中所含K+数目为2NA | |
| C. | 1 mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为N A | |
| D. | O2的摩尔体积约为22.4 L•mol-1 |
14.已知一些燃料的燃烧热的数据如表所示:
使用相同质量的上述燃料,产生热量最多的是( )
| 燃料 | 一氧化碳 | 甲烷 | 正戊烷 | 乙醇 |
| △H/(kJ•mol-1) | -283.0 | -891.0 | -3761 | -1366.8 |
| A. | 一氧化碳 | B. | 甲烷 | C. | 正戊烷 | D. | 乙醇 |
4.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | Na2CO3俗称纯碱,属于盐类,可用于洗涤油污等 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
11.下列物质,能使干燥的蓝色石蕊试纸先变红又褪色的是( )
①氯气②液氯③新制氯水④敞口放置的久置氯水⑤盐酸⑥用盐酸酸化的漂白粉溶液.
①氯气②液氯③新制氯水④敞口放置的久置氯水⑤盐酸⑥用盐酸酸化的漂白粉溶液.
| A. | ②③ | B. | ①②③④ | C. | ③⑥ | D. | ③④⑥ |
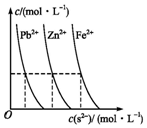 平衡指的是两个相反方向的变化最后所处的运动状态;中学阶段涉及的平衡有气体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等.
平衡指的是两个相反方向的变化最后所处的运动状态;中学阶段涉及的平衡有气体可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等.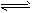 P(g)+Q(g),△H>0请回答下列问题:
P(g)+Q(g),△H>0请回答下列问题: